
Science Adv | 重庆医科大学段晨阳团队揭示脓毒症心肌病中的线粒体“甩锅”机制
脓毒症是由感染引起的一种危及生命的全身性炎症反应综合征,常导致多器官功能障碍,死亡率高达20%。其中约40%的患者会出现心肌功能障碍,表现为心室收缩力下降和射血分数降低。长期以来,研究主要关注心肌细胞本身的损伤与修复,然而最新观点认为,非心肌细胞如内皮细胞、成纤维细胞和巨噬细胞在维持心脏稳态中同样至关重要。这些细胞间的通讯机制,特别是线粒体转移,成为理解脓毒症心肌病发生发展的关键切入点。

·研究结果·
研究团队通过建立盲肠结扎穿刺小鼠脓毒症模型,结合单细胞RNA测序技术,分析了44289个心脏单细胞转录组数据。结果显示,脓毒症导致心脏内皮细胞、成纤维细胞和巨噬细胞发生显著的功能重塑。原本具有旺盛线粒体氧化代谢能力的Aqp7+内皮细胞逐渐消失,取而代之的是Cxcl2+和Metal+两个新亚群,这些细胞呈现活性氧积累、炎症反应增强和线粒体功能受损的特征。
在成纤维细胞中,依赖于脂肪酸代谢的Fmo2+亚群逐渐减少,而具有促炎特征的Lcn2+亚群显著增加。透射电镜观察发现,这些新出现的细胞亚群中都积累了大量的受损线粒体。通过 Seahorse 代谢分析证实,与原始亚群相比,这些新亚群的线粒体呼吸能力明显下降,基础呼吸和最大呼吸速率均显著降低。
巨噬细胞群体同样发生了类似转变。Hpgd+巨噬细胞逐渐减少,而Metal+巨噬细胞和Ccr2+巨噬细胞显著增多。SCENIC转录因子分析发现,Fosl1同时调控着Lcn2+成纤维细胞和Lcn2+单核细胞的出现,提示存在共同的调控机制。
考虑到非心肌细胞自身线粒体数量有限,研究团队推测这些细胞中受损线粒体的积累可能来源于心肌细胞转移。通过超高分辨率显微镜、Nanolive活细胞成像和扫描电镜观察,他们发现脓毒症后心肌细胞与周围内皮细胞、成纤维细胞和巨噬细胞之间形成了大量隧道纳米管结构。这些纳米管的长度和宽度均显著增加,且具有功能性运输能力,可介导线粒体和Drp1蛋白在细胞间转移。

脓毒症后心肌细胞和心脏驻留细胞之间受损线粒体中TNT形成、延伸和转移的超高分辨率成像
为探究Drp1在这一过程中的作用,研究团队构建了心肌细胞特异性Drp1敲除小鼠。结果显示,Drp1敲除后心肌细胞与周围细胞间的隧道纳米管形成明显减少,受损线粒体在非心肌细胞中的积累也显著降低。单细胞测序分析证实,原本在脓毒症中出现的Cxcl2+内皮细胞、Metal+内皮细胞、Lcn2+成纤维细胞和Metal+巨噬细胞等异常亚群在Drp1敲除后消失。功能检测显示,这些细胞的活性氧水平下降,线粒体呼吸能力恢复,心脏功能得到改善。
分子机制研究表明,脓毒症状态下Drp1与细胞骨架蛋白Filamin和Kinesin的相互作用显著增强。分子对接分析显示,Drp1与Filamin的结合自由能为-16.2 kcal/mol,结合位点位于GTP酶结构域;与Kinesin的结合自由能为-12.8 kcal/mol,结合位点位于MD结构域。结构光照明显微镜观察到,脓毒症刺激后Filamin和Kinesin在隧道纳米管中的分布由均匀排列转变为不连续的簇状聚集。通过长时间活细胞成像发现,野生型心肌细胞受刺激后,微丝和微管会动态向外延伸形成伪足,逐步建立功能性隧道纳米管并将完整线粒体转移给周围细胞;而Drp1敲除的心肌细胞则无法形成功能性隧道纳米管,伪足延伸不完全。
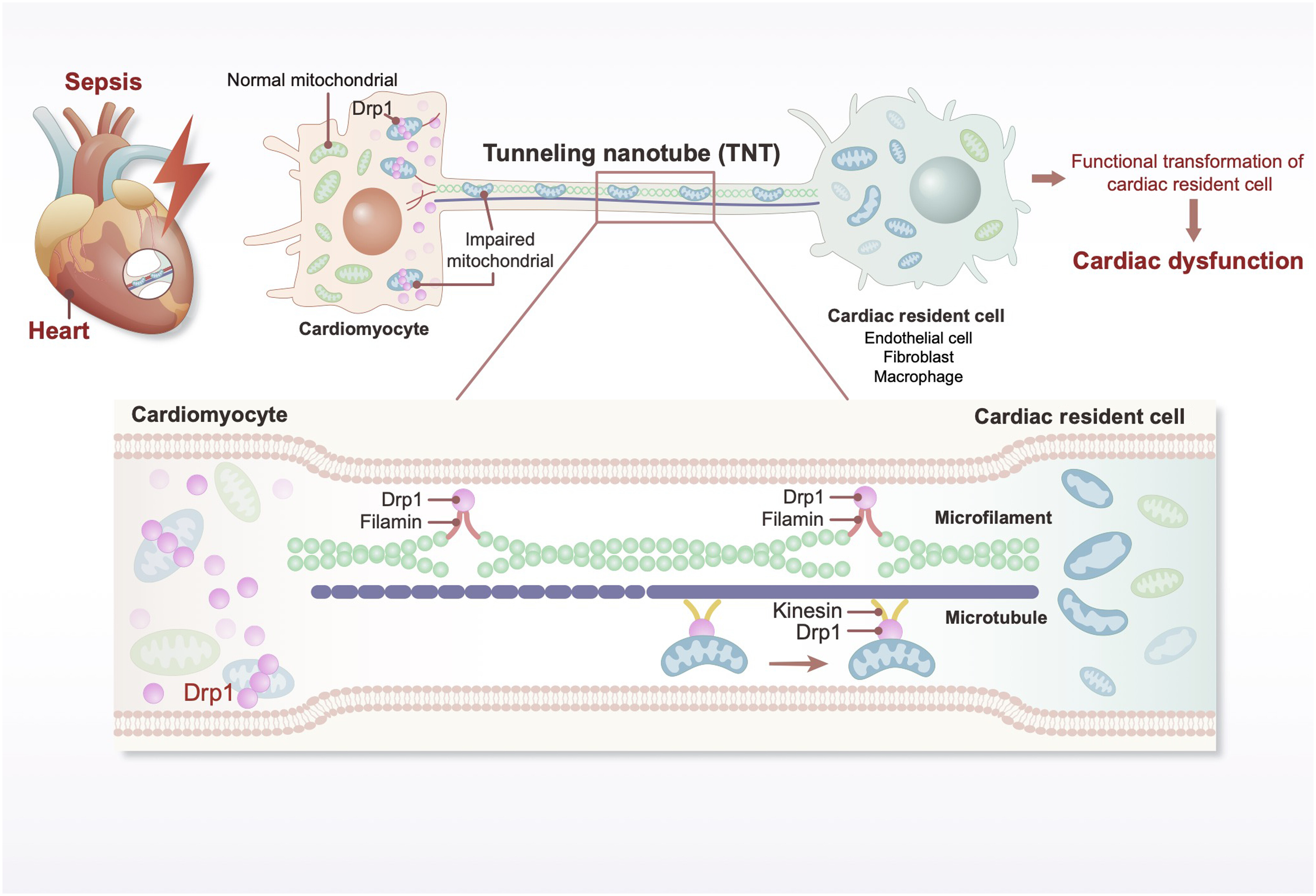
Drp1介导的TNT形成和线粒体转移在脓毒症后心脏功能障碍中的机制说明
原文链接:https://www.science.org/doi/full/10.1126/sciadv.adz3266

扫一扫,反馈当前页面
和元生物