
CAR-T 研发利器“提速降本”| CD19 CAR-T现货慢病毒限时6999元
在现代医学的漫长征程中,总有一些名字,会因为一场与死神的搏斗,被永远镌刻在历史里。Emily Whitehead,一个曾经被宣判 “只剩最后时光” 的白血病女孩,用一场惊心动魄的治疗,不仅为自己赢回了生命,更让 CAR-T 细胞疗法从濒临沉寂的实验室,走向全球临床,成为攻克血液肿瘤的 “终极武器”。
全球首例
CD19 CAR-T治疗白血病儿童患者
2010 年,5 岁的 Emily 被确诊为急性淋巴细胞白血病(ALL)。在很多人看来,儿童 ALL 是 “不幸中的万幸”,治愈率相对较高。可命运对 Emily 格外残酷,常规化疗、骨髓移植均告失败,医生一度建议临终关怀。绝境之中,她成为全球首位接受CD19 CAR-T治疗的白血病儿童患者【1】。2012年6月,Emily最终战胜了白血病,并正式出院。如今的 Emily,早已长成健康开朗的少女。她的笑脸,是 CAR-T 疗法最生动的 “活广告”,也是医学进步最温暖的见证。
2017 年 8 月,FDA 正式批准全球首款 CAR-T 疗法 ——诺华公司的 tisagenlecleucel(Kymriah),用于治疗 25 周岁以上难治性或 2 次及以上复发的 B 细胞前体 ALL。二期临床数据显示:63 例可评估患儿中,83% 的患者在输注 3 个月内达到完全缓解(CR)或不完全血细胞计数恢复(CRi)的CR【2】。这一批准,拉开了 CAR-T 时代的大幕。吉利德以 119 亿美元收购 Kite Pharma,布局淋巴瘤 CAR-T 产品;全球近 40 家企业与科研机构合作,加速研发针对更多肿瘤的 CAR-T 技术。从白血病、淋巴瘤到多发性骨髓瘤,这项 “活的药物”,为无数无药可治的晚期患者带来治愈希望。截止至2025年12月11日,全球共有15款CAR-T 获批产品,其中美国有7款,中国有8款。
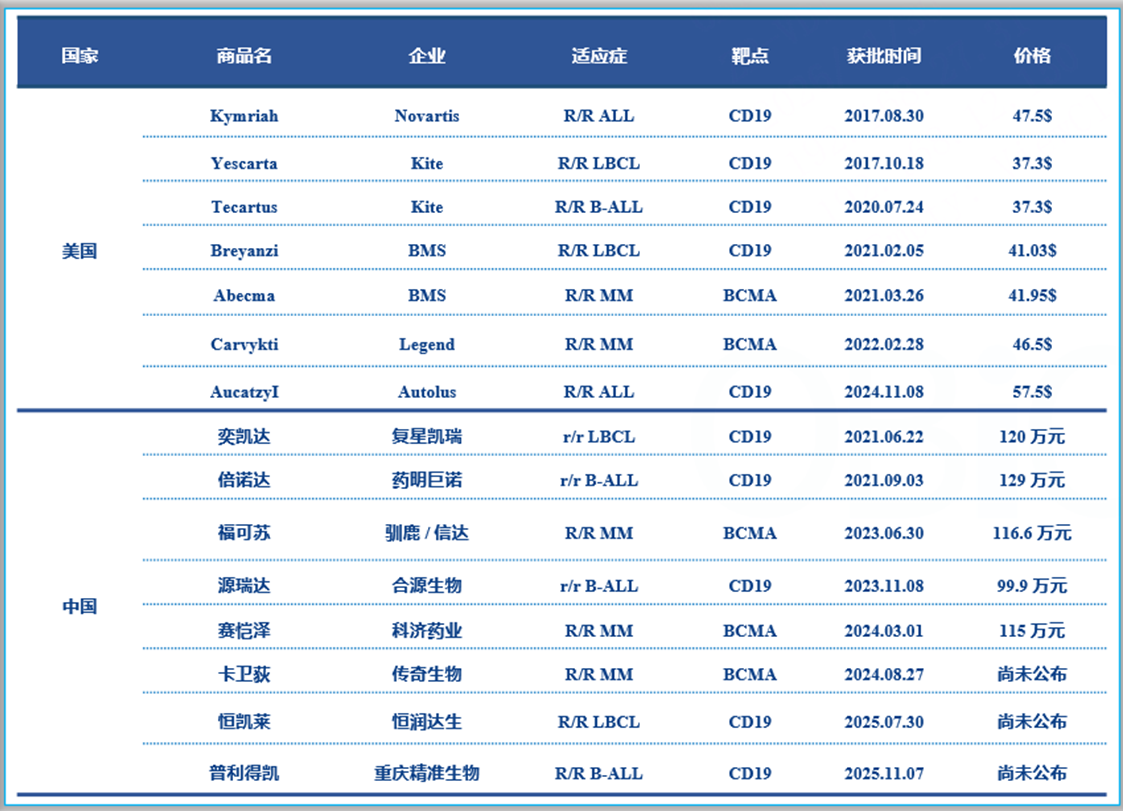
图1. CAR-T产品获批情况(和元整理)
·什么是CAR-T疗法?·
CAR-T(Chimeric Antigen Receptor T-Cell Immunotherapy)是指嵌合抗原受体T细胞免疫疗法。该方法是治疗肿瘤的新型精准靶向疗法,通过优化改良后在临床肿瘤治疗上取得了很好的效果。本质是把患者自身的 T 细胞取出,在体外装上能精准识别肿瘤 / 致病细胞的 “导航受体(CAR)”,从而能够识别并结合肿瘤抗原,然后在体外扩增 CAR-T 细胞,将 CAR-T 细胞输回患者体内,实现肿瘤细胞的精准杀伤。它的核心突破在于绕过 MHC 限制,直接识别细胞表面抗原。
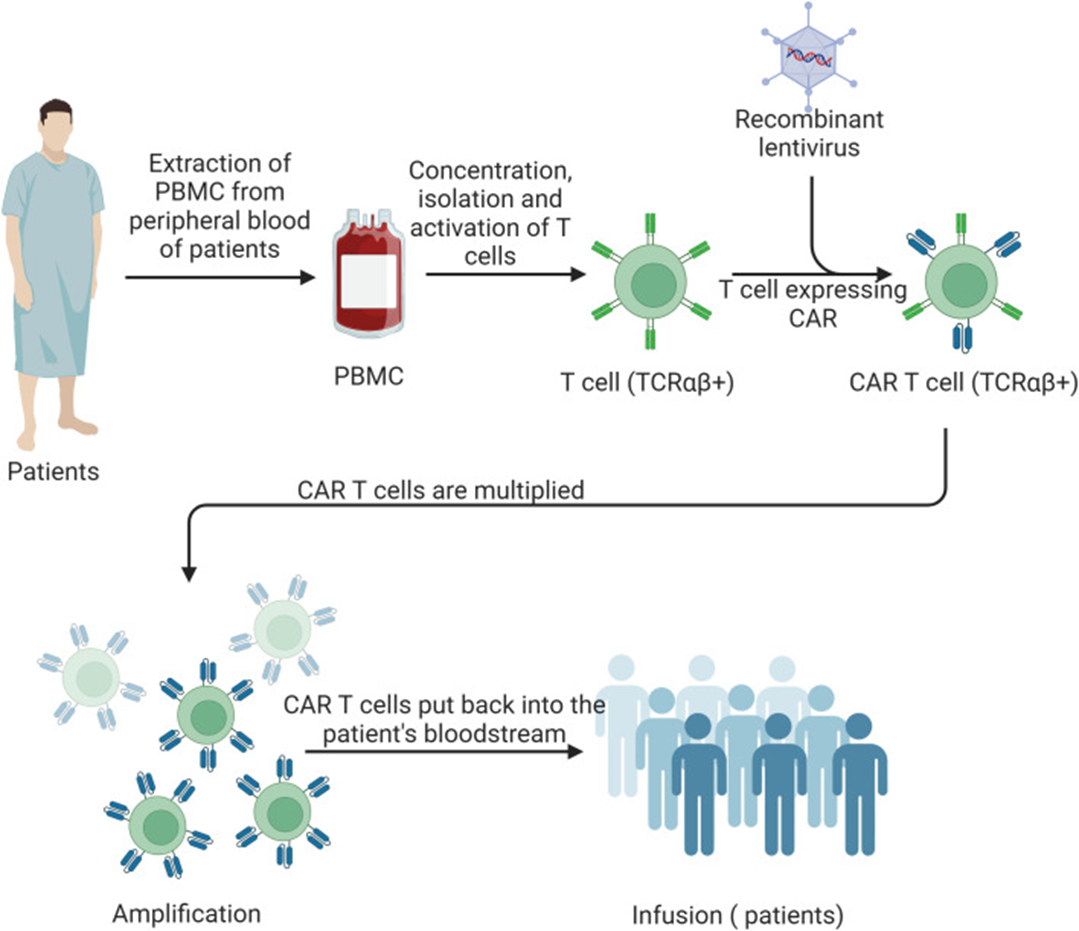
图2. CAR-T细胞疗法流程示意图[3]
·CAR的介绍·
嵌合抗原受体(CAR)是CAR-T的核心部件,赋予T细胞HLA非依赖的方式识别肿瘤抗原的能力,这使得经过CAR改造的T细胞相较于天然T细胞表面受体TCR能够识别更广泛的目标。CAR分子主要包括三部分:胞外域、跨膜域和胞内域。
胞外域:包括抗原识别结构域和铰链区
抗原识别结构域由单克隆抗体的可变重链(VH)和轻链(VL)通过连接体连接形成的 ScFv 构成。抗原识别结构域的主要功能是特异性识别靶细胞表面存在的肿瘤相关抗原(TAA),从而促进携带 CAR 的 T 细胞的激活。
铰链区(Hinge)的作用是增强 ScFv 的灵活性,克服空间位阻,促进 CAR 与靶抗原的结合。
跨膜结构域
跨膜结构域(TMD)是 CAR 的中间部分,由一个跨越细胞膜并将细胞外和细胞内结构域连接起来的疏水α-螺旋组成。其作用包括将 CAR 锚定在细胞膜上并将激活信号传递到细胞内结构域。
胞内域:包括共刺激结构域和信号转导结构域
共刺激结构域(CM)位于 T 细胞活化区,对 T 细胞活化至关重要,因为它通过共刺激分子和细胞内信号传导促进双重活化。最常见的共刺激结构域是 CD28 和 4-1BB。包含 CD28 共刺激结构域的 CARs 表现出更快、更强烈的信号活性,可促进 T 细胞分化为效应记忆 T 细胞,并促进有氧糖酵解。而含有 4-1BB 共刺激结构域的 CARs 具有更慢、更渐进的活性特征,可延长 T 细胞的寿命并维持其抗癌作用,可驱动 T 细胞分化为中央记忆 T 细胞,促进线粒体产生、增强呼吸作用,并促进脂肪酸氧化。
信号转导结构域通常为T细胞受体TCR/CD3ζ链或免疫球蛋白Fc受体FcεRIγ链,含有免疫受体酪氨酸活化基序(ITAMs),ITAM是典型的免疫受体激活域,当CAR的抗原识别结构域与肿瘤细胞表面的抗原结合后,会触发CD3ζ的免疫受体酪氨酸激活基序(ITAMs)发生磷酸化,这一磷酸化过程会招募并激活ζ链相关蛋白激酶70 (ZAP-70) 的信号转导[4],从而促进下游接头蛋白和支架蛋白的组装,激活T细胞反应(增殖、细胞因子释放等)。
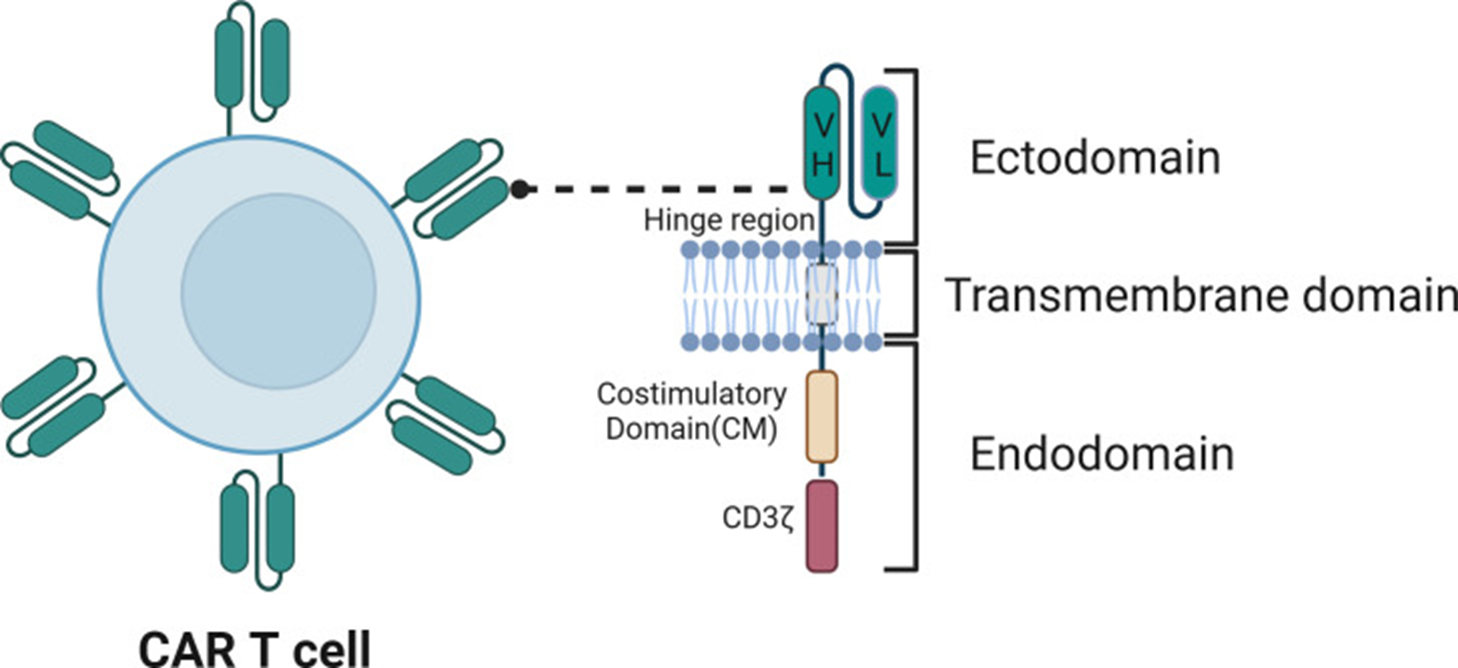
图3. CAR结构示意图[3]
·CAR的代际演变·
第一代CAR
第一代 CAR 由单链抗体 scFv、铰链区、跨膜区以及CD3ζ (常用)或 FcεRI胞内信号结构域组成,该结构域是 TCR 信号的主要传导元件,可启动级联信号。借助 CD3ζ 信号能够完成 T 细胞活化,发挥细胞毒性作用并分泌 IL-2 等细胞因子,从而有效杀伤肿瘤细胞。
核心缺陷:1.无法产生足量 IL-2 以支持长期增殖,需外源性补充 IL-2;2.缺乏共刺激信号,T 细胞活化不充分;3.体内增殖短暂、细胞因子分泌有限,易发生凋亡,抗肿瘤效果受限。
第二代CAR
第二代在第一代基础上新增一个共刺激结构域(最常用CD28 或 4-1BB),与 CD3ζ 串联。这一改造使 T 细胞同时获得抗原刺激信号与共刺激信号,显著促进 IL-2 合成与 T 细胞充分活化,在增殖、存活、细胞毒性与体内持久性上全面优化。目前,第二代 CAR-T 是当前临床主流,上市的CAR-T药物均为二代产品。
第三代CAR
第三代CAR搭载两个及以上共刺激结构域(与 CD3ζ 串联),最经典组合为CD3ζ-CD28-4-1BB,还可整合 OX40(CD134)等。多共刺激信号可激活 JNK、ERK、NF-κB 等通路,增强 T 细胞抗肿瘤活性、增殖能力、存活时间,并提升 IL-2、TNF-α、IFN-γ 等细胞因子分泌。
临床表现:体外与动物实验显示,第三代CAR在 B 细胞非霍奇金淋巴瘤中扩增更强、存续更久,抗肿瘤效力优于第二代;但安全性未提升甚至更差,单纯叠加共刺激分子并未带来预期的疗效增益。
第四代CAR
又称TRUCK(精准型 CAR-T / 装甲 CAR-T),在第二代基础上新增NFAT(活化 T 细胞核因子)转录调控元件,并整合可诱导自杀基因,可在肿瘤微环境中定向分泌细胞因子(主要为 IL-12),招募并激活天然免疫细胞,克服免疫抑制;并且促进 CAR-T 向肿瘤组织浸润,更适配实体瘤治疗;自杀基因可调控 CAR-T 在体内存活时间,降低细胞因子风暴等严重毒副作用。
第五代CAR
第五代在第二代的基础上,添加细胞质IL-2受体β链(IL-2Rβ)结构域和STAT 3结合片段。激活第五代可促进T细胞受体(TCR)和细胞因子驱动的JAK-STAT信号传导,增强生物工程细胞的增殖和活化T细胞。
另外,已有研究利用CRISPR-Cas9基因编辑技术开发出了新一代异体通用型CAR-T疗法,成功治疗了自身免疫病患者,这标志着CAR-T疗法在治疗非肿瘤性疾病方面的巨大潜力。此外,CAR-T疗法的靶点也在不断拓展,从CD19扩展到BCMA等其他靶点,以适应不同类型的癌症治疗需求。未来,随着基因编辑技术、合成生物学的发展以及靶向性mRNA递送技术的突破,CAR-T疗法有望在更多疾病领域展现其治疗潜力。
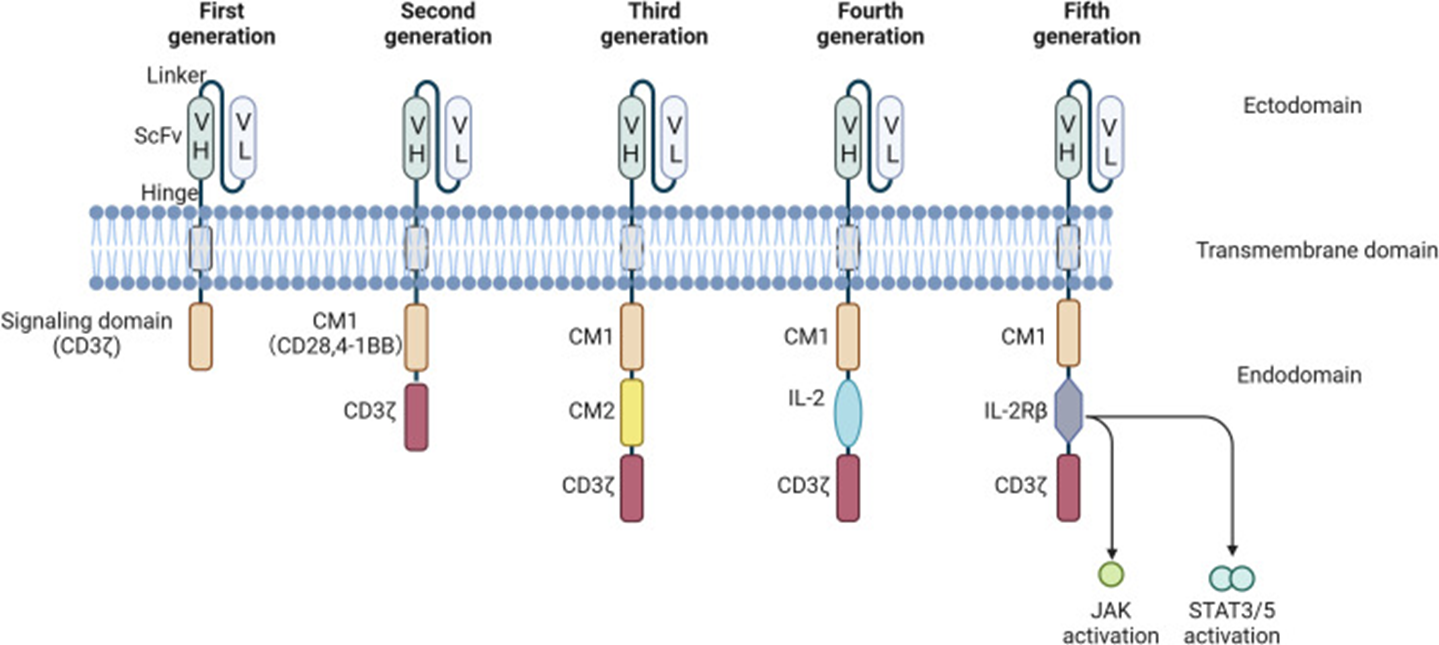
图4. CAR的发展历程[3]
·和元生物CD19 CAR-T 现货慢病毒·
·限时特价6999元·
|
CD19 CAR-T现货慢病毒产品载体信息 |
|
LV-EF1α-CD19 scFv-2ndCAR(CD28) |
|
LV-EF1a-CD19 scFV-2ndCAR(4-1BB) |
|
LV-EF1a-CD19 scFV-3rdCAR(CD28&4-1BB) |
(For research only)

1. PMID: 28902570
2.https://pps.cpu.edu.cn/cn/article/pdf/preview/e40a4210-f7c7-40e1-be1d-8ad0e0ac4c9c.pdf
3. PMID: 39850899
4. PMID: 36209106

扫一扫,反馈当前页面
和元生物