全国服务热线400-151-5198 业务咨询15800353038
化学遗传学技术(或称药理遗传学技术)是近年来与光遗传学一起出现的重要新技术。该技术通过对一些生物大分子实行改造,使其能和先前无法识别的小分子进行相互作用,从而达到可控、可逆(可以随时加入或除去化合物,从而启动或中断特定的反应)控制生物大分子的活性,该技术已经在信号转导、药物开发、功能基因组学等方面的研究中得到了广泛的应用。
目前已改造的生物大分子包括核酸杂交、蛋白质激酶、各种代谢酶和G蛋白耦联受体(G protein‒coupledreceptors,GPCRs)。现在有很多基于GPCRs改造的化学遗传学平台,例如1991年构建的基因编码受体的等位基因特异激活(Allele-specific activation of genetically encoded receptors)、1998年构建的只能被合成配体激活的受体(Receptorsactivated solely by synthetic ligands, RASSLs)、基因工程改造的受体(Engineered receptors)和2007年构建的只由特定药物激活的受体(Designer receptors exclusively activatedby designer drugs,DREADDs)。其中,DREADDs已成为应用最广泛的化学遗传学技术。
DREADD技术被广泛用于以细胞特异性、无创地增强或抑制神经元的活动。虽然DREADD缺乏像光遗传学那样精准的时间控制能力,但是由于在进行疾病治疗时,最有可能需要的是长期神经元环路调节,而DREADDs会非常适合这类应用。此外,许多FDA批准药物的目标作用目标是GPCRs,而DREADDs是改造过的GPCRs,因此DREADDs可能会在药物开发方面提供丰富的可能性。
DREADDs技术
DREADDs技术是由Bryan L. Roth等人发明的,他们改变了G蛋白偶联受体—乙酰胆碱受体的结构,改变后其只能被特定的化合物Clozapine-N-oxide(CNO)激活或者抑制。此类改变的受体会选择性地作用于不同的GPCR级联反应,包括Gq、Gi、Gs、Golf和β-arrestin,其中应用最广泛的是Gq-DREADD和Gi-DREADD。通过将上述受体在细胞内表达,在CNO的作用下,其产生的结果各不相同。
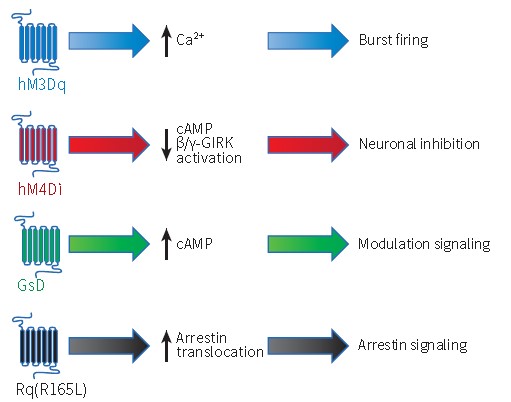
常用DREADDs受体作用原理
(Scott M. Sternson & Bryan L. Roth, Annu. Rev. Neurosci., 2014)
常见的DREADDs受体
最初的Gq-DREADD即hM3Dq,改造自人毒蕈碱型乙酰胆碱受体(the human muscarinic acetylcholine receptor,mAchRs)亚型M3(也称为hM3)。在正常生理状况下,hM3和乙酰胆碱结合,然后和Gq类G蛋白耦合受体耦合,作用于磷脂酶C、肌醇三磷酸和胞内钙离子这一信号通路。
令人吃惊地是,只要将Y3.33C和A5.46这两个位点突变,就能使hM3受体不能和乙酰胆碱耦合,但是会和纳摩尔浓度级别的CNO结合,这种突变后的hM3受体被命名为hM3Dq (human M3 muscarinic DREADD receptor coupled to Gq)。
在不同的细胞类型中,CNO诱导hM3Dq的结果是不一样的,比如:1) 在成熟神经元中,CNO诱导hM3Dq的结果是将神经元去极化(depolarization),加强神经元的兴奋性,这也是hM3Dq最常用的功能,即促使神经元的放电活动;2) 在星形胶质细胞中,有人报道CNO诱导hM3Dq的结果是增加星形胶质细胞Ca+的释放,从而改变自主神经系统的生理条件;3) 在神经系统以外,也有一些研究,例如在胰腺Β细胞表达hM3Dq,急性CNO处理会促进胰岛素的释放,而慢性CNO处理导致Β细胞数目增加;在肝细胞中,激活hM3Dq会增加血糖水平,也许是因为糖原分解和糖异生作用增加。
Y3.33和A5.46在不同的人毒蕈碱型乙酰胆碱受体亚型中是保守的,因此科学家同样可以突变M2和M4 mAchRs上的Y3.33、A5.46位点,由于M2、M4的下游激活的是Gi通道,于是产生Gi-DREADDs,命名为hM2Di和hM4Di,他们可以激活Gi调节的信号通路。
Gi耦合的GPCRs可以激活G蛋白内向整流钾通道(GIRK),在CNO的作用下, hM2Di和hM4Di受体被激活可以抑制神经元的放电活动,其中使用最多的Gi-DREADD是hM4Di。也有研究表明,hM4Di可以抑制神经递质的释放,从而达到抑制神经元活动的效果。
DREADDs技术的应用策略
借助病毒载体的DREADDs技术应用一般包括以下几个关键步骤:
1、根据实验目的,确定合适的DREADDs受体,一般来说,激活神经元选择hM3Dq,抑制神经元选择hM4Di;
2、借助病毒载体在动物体内表达DREADDs受体;
3、设计实验方案,在合适的时间窗口内给予动物CNO药物,激活受体,给予CNO的方式包括脑内定位注射、腹腔注射和喂水;
4、表型检测,通过行为学或电生理手段等检测神经元活动变化带来的变化。
DREADDs技术优势
1、实验要求较低,操作简单:不像光遗传学技术需要光纤、激光控制器等,DREADDs技术只需常规药理学技术手法,注射或者喂食CNO即可。
2、非侵入性:不像光遗传技术需进行开颅手术埋置光纤,因此不会因为额外负重影响小鼠行为,可实现在小鼠完全自由活动的情况下调控特定脑区和特定神经元的活动。
3、实现长时间激活或抑制神经元活动:由于两种技术原理不同,光遗传学技术依赖的是光敏感通道的开放,是需要离子在细胞膜上的流动产生电位变化,影响神经元活动,而长时间离子逆浓度差进出细胞需消耗大量ATP(如离子泵),这会导致细胞受损死亡,此外光刺激的热效应同样会损伤细胞。相比之下,DREADDs表达的是一种受体,可以长达数小时持续激活或抑制神经元活动而不影响细胞正常生理。
4、安全性高:CNO是FDA批准上市药物-氯氮平的代谢产物,体内应用相对安全。此外,许多FDA批准药物的目标作用目标是GPCRs,而DREADDs是改造过的GPCRs,因此DREADDs可能会在药物开发方面提供丰富的可能性。
DREADDs技术应用案例
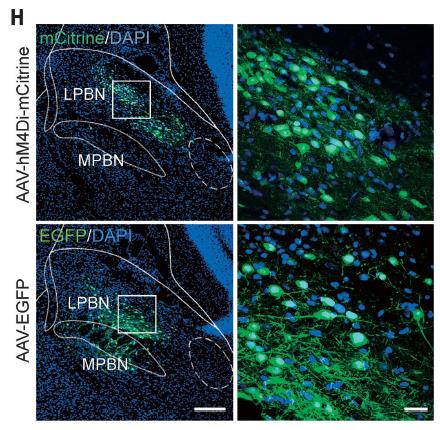
①客户发表文章:Science. (IF=41.058). Mu D,et.al. (2017). A central neural circuit for itch sensation. [AAV,痒, 光遗传,化学遗传]
注射部位:小鼠PBN
载体:AAV-hSyn-HA-hM4Di-IRES-mCitrine
血清型:AAV2/9
病毒滴度:1E+13 VG/mL
注射体积:150nl
观察时间:3周
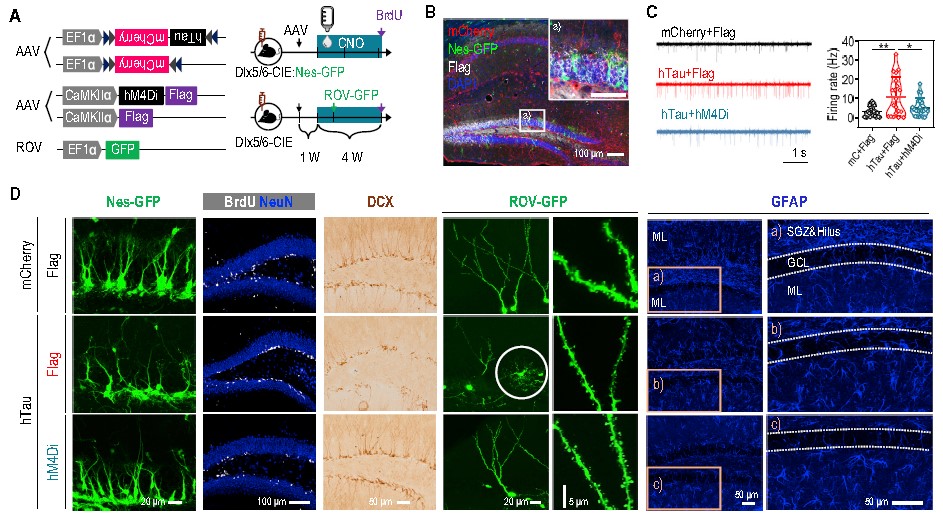
②客户发表文章:Cell Stem Cell. (IF=21.464). Jie Zheng, et al. (2020) Interneuron Accumulation of Phosphorylated tau Impairs Adult Hippocampal Neurogenesis by Suppressing GABAergic Transmission. [AAV,AD,化学遗传]
注射部位:小鼠海马DG
载体:AAV-CaMKIIa-hM4Di
病毒滴度:3E+12 VG/mL
注射体积:300nl
观察时间:4周
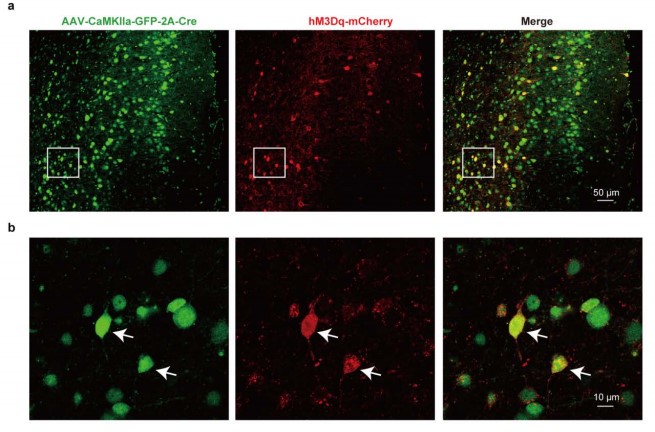
客户发表文章:Science. (IF=41.058). Mu D,et.al. (2017). A central neural circuit for itch sensation. [腺相关病毒, 痒, 光遗传,化学遗传]
注射部位:小鼠ACC
载体:AAV-EF1a-DIO-hM3D(Gq)-mCherry
血清型:AAV2/8
病毒滴度:3E+12VG/mL
注射体积:350nl
观察时间:3周