一、钙离子成像技术(Calcium imaging)
钙离子成像技术(Calcium imaging)是指利用钙离子指示剂监测组织内钙离子浓度的方法。在神经系统研究中,我们常用钙离子成像技术监测神经元内钙离子的变化,提示神经元活动。有了钙成像技术,原本悄无声息的电生理活动就变成了一幅形象地、斑斓闪烁的壮观影像,研究人员可以同时大量追踪神经元活动,研究其关系,因而被全世界神经科学家们追捧。
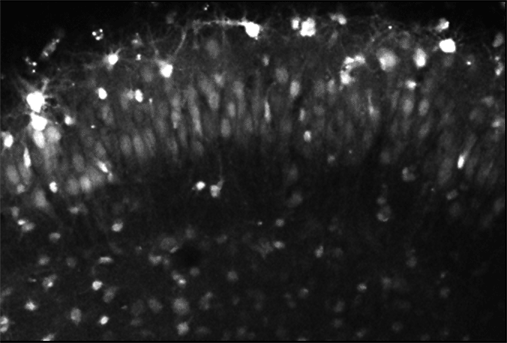
图1.钙离子成像技术
1)钙离子成像技术原理
在生物体内,钙离子是细胞信号产生的基础,在很多功能方面有重要作用。在哺乳动物的神经系统中,钙离子是一类重要的神经元胞内信号分子,神经元静息状态下,胞内钙离子浓度约为50-100nM,而当神经元活动的时候,胞内钙离子浓度能上升10-100倍,而钙离子对于突触囊泡释放必不可少;神经元在放电的时候会爆发出一个短暂的钙离子浓度高峰,这意味着神经元钙离子浓度表征突触传递和神经元活动。
图2 神经元钙离子浓度表征突触传递和神经元活动示意图
因而,神经元钙离子成像技术的原理就是借助钙离子浓度与神经元活动之间的严格对应关系,利用特殊的荧光染料或者蛋白质荧光探针(钙离子指示剂,Calcium indicator),将神经元中钙离子的浓度通过荧光强度表现出来,并被显微镜捕捉,从而达到监测
神经元活动的目的(图3)。
因而,钙离子成像技术的核心在于钙离子指示剂,现在广泛使用的钙离子指示剂有化学性钙离子指示剂(chemical indicators)和基因编码钙离子指示剂(genetically-encoded indicators)两类:
1、化学性钙离子指示剂:指的是可以螯合钙离子的小分子,所有这些小分子都基于BAPTA(氨基苯乙烷四乙酸),BAPTA能够特异性地和钙离子螯合,而不会和镁离子螯合,所以被广泛地用作钙离子螯合剂。目前较为成熟的化学性钙离子指示剂包括Oregon Green-1、Fura-2、Indo-1、Fluo-3、Fluo-4。
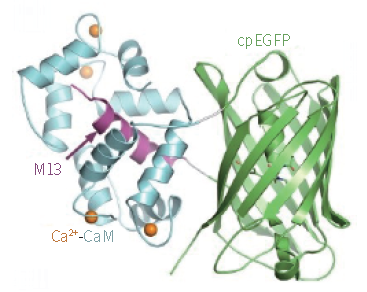
2、基因编码钙离子指示剂:这些指示剂是来自于绿色荧光蛋白(GFP)及其变异体(例如循环排列GFP、YFP、CFP)的荧光蛋白质,与钙调蛋白(CaM)和肌球蛋白轻链激酶M13域融合。现在使用较广泛的基因编码钙离子指示剂有:GCaMP、Pericams、Cameleons、TN-XXL和Twitch,其中GCaMP6由于它有着超强的敏感度,现在被广泛应用于活体钙成像研究,其发出荧光的原理在于钙离子浓度上升导致M13与CaM结合,从而改变cpEGFP的构象,将其从无荧光的状态变为绿色荧光
图3 GCaMP蛋白的基本结构和原理(来自WIKI)
2)常见的钙离子指示剂
1、GCaMP6系列:
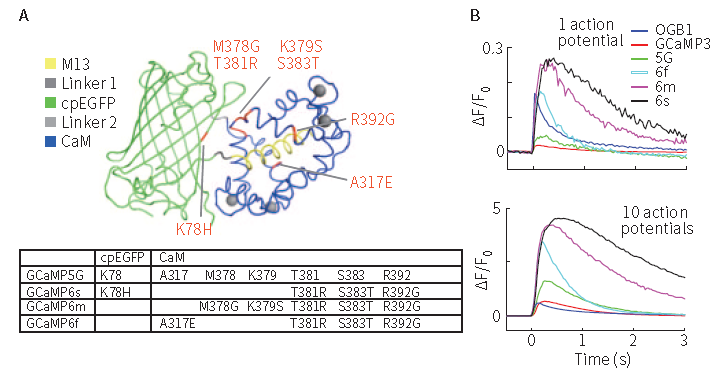
第六代GCaMP蛋白(GCaMP6)有三种不同亚型:GCaMP6s、GCaMP6m、GCaMP6f,其特点各不相同(图4)。GCaMP6s高敏感,适合低频信号的指示,;GCaMP6f有快速动力学曲线,解离最快,适合高频信号的指示,需要根据实验需求进行选择。
图4 几种不同GCaMP蛋白的特性(Douglas S. Kim, et al., Nature, 2013)
2、jGCaMP7家族:
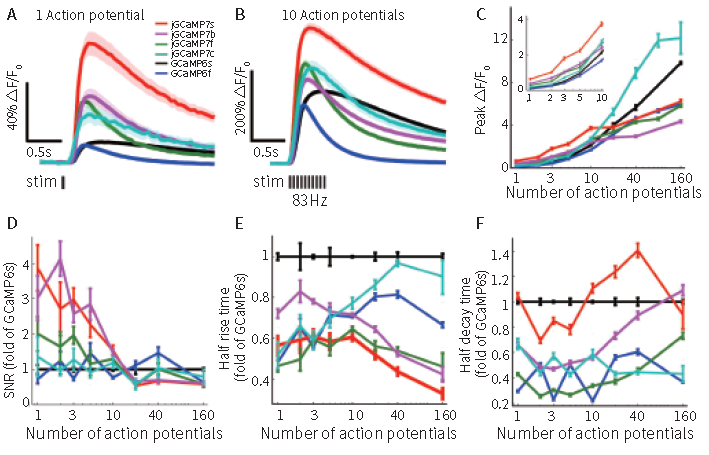
jGCaMP7(Janelia GCaMP7,区别于过去出现过的G-CaMP7)。包括四类不同特点的蛋白:jGCaMP7s、jGCaMP7f、jGCaMP7b、jGCaMP7c(图5)。jGCaMP7s高敏感;jGCaMP7f具有快速动力学曲线,适用于更强的检测单动作电位反应或群里活动实验;jGCaMP7b具有较明亮的背景荧光,适用检测神经元突起或神经纤维;jGCaMP7c的本底荧光最低,对比度高,信号清晰,适用于大范围成像。
图5 jGCaMP7蛋白的反应特点(Douglas S. Kim, et al., bioRXiv, 2018)
3、XCaMP系列:
基于CaMKK为骨架,通过一系列的突变筛选,包括四种不同颜色:蓝色的XCaMP-B,绿色的XCaMP-G,橙色的XCaMP-O和红色的XCaMP-R(图6)。其中XCaMP-G的荧光强度比GCaMP6强,动作电位刺激诱发的钙离子反应性能也比GCaMP6有明显提高。结合特定的神经元特异的表达方法,可实现在自由活动状态下同时监测特定行为中三种不同神经元类型的活动;结合双光子显微镜,进行微结构功能成像,实现对突触前和突触后结构同时双色成像。
图6 XCaMP蛋白特点(Haruhiko Bito’s, lab.,cell, 2019)
4、CaMPARI:
一种能够兼顾全局和微观的新型钙成像技术, 包含CaMPARI以及CaMPARI2(第二代)。其原理在于,CaMPARI蛋白在正常状态下会发出绿色荧光,而如果对这种蛋白同时使用高浓度钙离子与紫外光处理,它就会不可逆、永久地转变成另一种能发出红色荧光的构象,即实现将瞬间的神经元活动变成永久的红色荧光蛋白表达(图7)。研究人员通过转基因技术将这种新型蛋白导入到实验动物的神经系统中,然后用高强度的紫外光照射动物的大脑,通过检查荧光,找到发红色荧光的神经元,这些神经元即是在紫外光照射期间活跃的神经元。由于紫外光可以对着整个大脑进行照射,所以理论上,人们可以对全脑进行检查。
图7 CaMPARI技术原理(Eric R. Schreiter, et al., Science, 2015)
5、jRGECO1a&RCaMP:
红色的钙离子敏感蛋白,可以同GCaMP一起使用,标记同一小鼠同一脑区两类细胞的活动不同的神经元类型。
6、GCaMP-X:
无损伤钙离子探针,可保护依赖于L型钙通道的兴奋-转录耦合免受干扰,同时仍表现出部分GCaMP的优良Ca2+感应特性。
更多钙离子技术病毒工具请搜索。。。(考虑加搜索框)
二、电压成像(voltage imaging)
细胞内钙离子浓度变化和细胞膜电位的变化是细胞活动的两个重要指标,由于钙信号衰减较慢,并不能充分表征神经元的动作电位,而且阈值以下的电压信号完全被忽略,于是科学家们利用细胞膜电位改变作为信号进行荧光成像。
1)电压成像技术原理
细胞膜电位变化是细胞活动最基本的信号,当膜电位变化时,细胞膜上镶嵌的许多蛋白质分子都会改变形状,这类随膜电位改变形状的蛋白分子叫电压敏感元件。而电压成像技术原理就在于将电压敏感元件和荧光蛋白连接起来,当膜电位改变时,电压敏感蛋白的改变就会影响荧光蛋白的结构,从而改变了后者的发光特性。这样就可以利用荧光来看神经细胞膜的膜电位变化了。
遗传编码的荧光电压指示剂(Genetically encoded voltage indicators, GEVIs)改造于一种细菌能吸收阳光的蛋白质--古紫质Archaerhodopsin,其能随着细胞膜电位改变发出荧光。通过GEVIs我们可以成像神经元的快速放电信号与阈下电活动,能实时监测细胞膜电位的波动,相比于钙指标,更能直接反映神经元的活性。
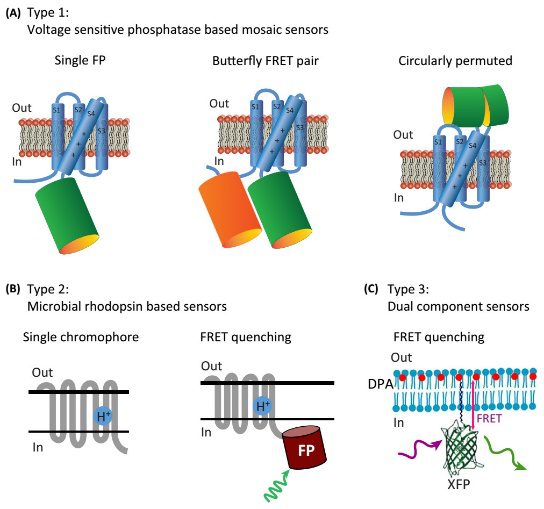
图8 三种类型GEVIs的示意图(Storace, D., et al., Trends Neurosci, 2016)
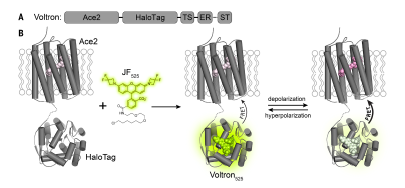
Voltron,是一种新型电压指示剂,不同于传统的GEVIs依赖于微生物视紫红质或荧光蛋白(这些荧光基团缺乏亮度与光稳定性),Voltron利用明亮且耐光型的合成染料。其原理在于Voltron将电压敏感性微生物视紫红质结构域和自标记蛋白标记域结合染料结合,后者可共价结合一种人工荧光染料配体,合成染料给药方式简单,且可跨血脑屏障。体内同时成像神经元的数量扩大10倍,且成像时间更加持久。
图9 Voltron结构的示意图(Eric R. Schreiter’s lab., science, 2019)
神经元功能成像是探究神经元编码各种功能的重要科学手段,广泛应用于神经生物学等各个研究领域,目前最常用方法为钙成像和电压成像。得益于双光子成像技术,通过记录细胞内钙离子浓度变化或细胞电位变化,实时反应细胞活动,实现了一系列行为动物活体动态功能成像技术!
三、神经递质荧光探针
在已知宇宙中,脑可能是最复杂的物体之一。根据前人的估计,我们的脑大约有1010-1012个神经元和1011-1013个胶质细胞,同时每个神经元拥有103-104个突触与其他神经元形成联系。神经递质作为突触间传递信息的重要“信使”,在神经元与细胞之间的通讯交流中起到关键的媒介作用,神经递质的紊乱常常伴随各种疾病的发生。因此,对神经递质的探测追踪是研究大脑功能和相关疾病的重要环节。然而,如何在拥有数十亿个神经细胞、数万亿个突触连接的大脑中精确检测神经递质的释放,是长久以来困扰科学家的一个难题。
北京大学李毓龙团队利用可与神经递质相结合的G蛋白偶联受体作为探针的骨架,将荧光蛋白(cpEGFP)与特异性的人源神经递质受体巧妙地进行分子水平的融合和改造,成功开发出新型可遗传编码的一系列神经递质荧光探针。
1)神经递质荧光探针原理
这一系列神经递质探针原理类似,都是基于人源神经递质受体,其原理在于把cpEGFP嵌入特定的神经递质受体,受体与神经递质结合后会引发受体构象改变转换为荧光信号(图10)。
目前通过病毒注射、转染等技术手段,可以将这种可遗传编码的探针表达在细胞或小鼠脑部,借助成像技术,观察神经递质浓度的实时变化。这类神经调质探针具有极高的灵敏度、分子特异性、精确的空间分辨率和亚秒级响应速度,已在果蝇、斑马鱼。小鼠脑部十几种神经元上得到验证,这将为研究大脑的功能以及神经系统疾病机制的解析提供重要的工具。
图10 GACh原理(Yulong Li’s lab., Nat Biotechnol, 2018)
2)常见的神经递质荧光探针
1、DA
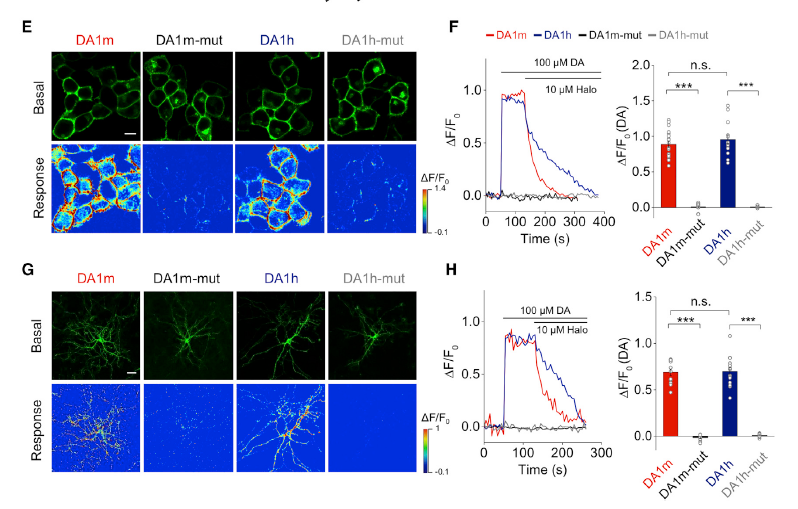
多巴胺是大脑中一种重要的神经递质,调控包括学习、记忆、运动等一系列关键功能,多巴胺失调会导致精神疾病或神经退行性疾病,多巴胺探针包含:DA1h和DA1m两种版本,分别对应高/低亲和力,适用于多巴胺释放量不同的脑区(图11)。
图11 GRABDA sensors表达在细胞和神经元中(Yulong Li’s lab., cell, 2018)
2、Ach
乙酰胆碱是人类发现的第一种神经递质,负责调节睡眠、成瘾、学习记忆等过程。乙酰胆碱信号传递失常,会导致先天性肌肉萎缩、糖尿病、阿兹海默症等疾病。GACh2.0对生理浓度乙酰胆碱具有高信噪比、高灵敏性的光学信号变化响应,并且具有亚秒级动力学及高度分子特异性,可实现对时空特异性乙酰胆碱信号的精确指征(图12)。
图12 GACh2.0 sensors特性(Yulong Li’s lab., Nat Biotechnol, 2018)
3、NE
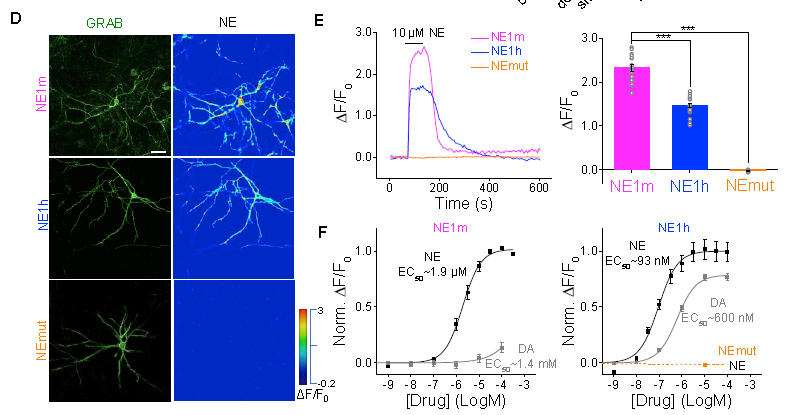
去甲肾上腺素作为一种重要的单胺类神经递质,参与感觉信号的调节、注意力调控、睡眠于觉醒、学习记忆等生理过程,去甲肾上腺素释放或信号传递的受损与一系列的精神疾病和神经退行性病变息息相关。去甲肾上腺素探针包含:NE1m和NE1h两种版本,分别对应高/低亲和力,适用于检测局部突触传递和非局部非突触传递的去甲肾上腺素释放(图13)。
图13 GRABNE sensors表达神经元(Yulong Li’s lab., Neuron, 2019)
此外,李毓龙教授团队正在积极开发更多新的神经递质、神经肽等荧光探针。
更多请搜索。。。(考虑加搜索框)
成像技术应用案例
1、GCaMP6f
客户发表文章:Science. (IF=41.058). Ren S,et.al. (2018). The paraventricular thalamus is a critical thalamic area for wakefulness. [腺相关病毒, 觉醒]
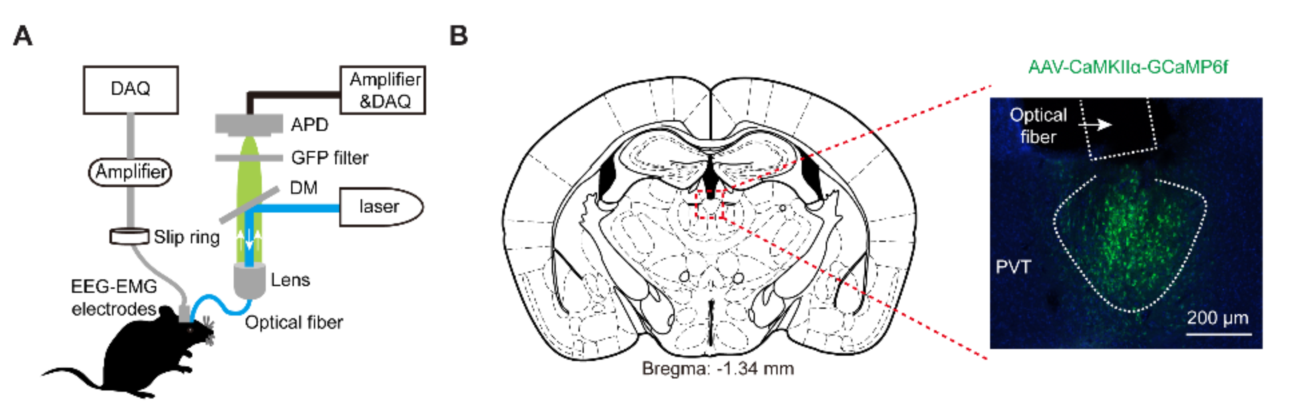
注射部位:小鼠PVT
载体:AAV-CaMKIIα-GCaMP6f
注射体积:100nl
观察时间:4周
2、GCaMP6s
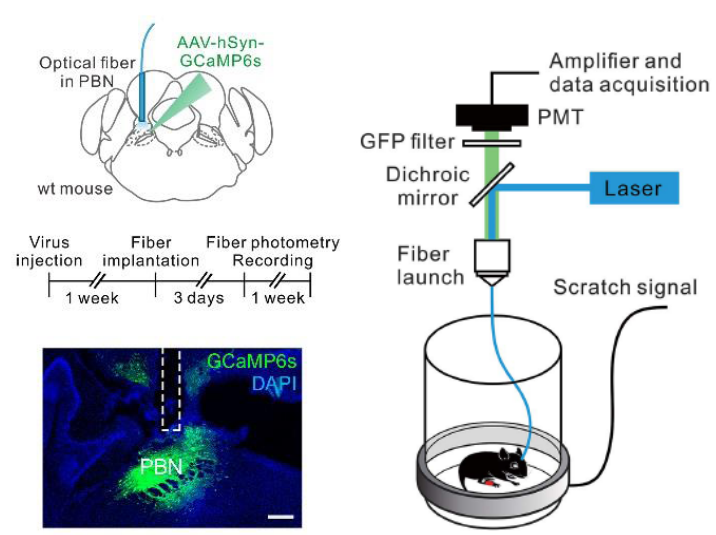
① 客户发表文章:Science. (IF=41.058). Mu D,et.al. (2017). A central neural circuit for itch sensation. [腺相关病毒, 痒, 光遗传, 化学遗传,钙成像]
注射部位:小鼠PBN
载体:AAV-hSyn-GCaMP6s
血清型:rAAV2/9
病毒滴度:5.3x1012 VG/mL
注射体积:300nl
观察时间:3周
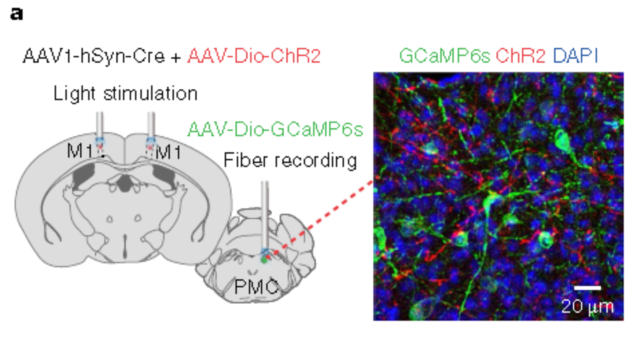
② 客户发表文章:Nature Neuroscience. (IF=19.912). Yao J,et.al. (2018). A corticopontine circuit for initiation of urination. [腺相关病毒, 神经环路]
注射部位:小鼠皮层M1、PMC
载体:rAAV2/1-hSyn-Cre&rAAV2/9-DIO-hChR2(H134R)-mCherry、rAAV2/9-DIO-GCaMP6s
病毒滴度:rAAV2/1: 5 × 1012 VG/mL;rAAV2/9-DIO-hChR2:1.2 × 1013 VG/mL;rAAV2/9-DIO-GCaMP6s:0.5 × 1012 VG/mL
注射体积:多点注射,每位点30-40nl
观察时间:4周
3、GCaMP5G
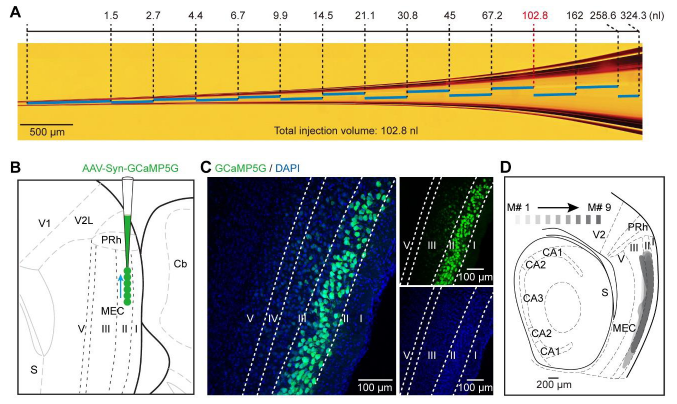
客户发表文章:Neuron. (IF=14.319). Han Q,et.al. (2018). A Visual-Cue-Dependent Memory Circuit for Place Navigation. [AAV, 学习与记忆, 钙成像]
注射部位:小鼠MECII
载体:pAAV-Syn-GCaMP5G
血清型:rAAV2/9
注射体积:约100nl
观察时间:4周