
Nat Neurosci | 浙大周煜东/沈逸团队揭示高脂饮食“吃到停不下来”的神经炎症机制
高热量食物会引起肥胖,然而人们总是管不住贪吃的嘴,对高热量食物欲罢不能,这其中的神经炎症机制暂不清晰。
2022年8月1日,浙江大学脑科学与脑医学学院周煜东/沈逸课题组在Nature Neuroscience杂志上发表“Diet-induced Inflammation in the Anterior Paraventricular Thalamus Induces Compulsive Sucrose-seeking”的研究论文,揭示了高脂饮食(high-fat diet, HFD)引发强迫性进食的神经炎症机制。研究发现高脂饮食可诱导小鼠丘脑室旁核前侧(anterior paraventricular thalamus, aPVT)小胶质细胞激活从而引发aPVT兴奋性神经元活动增加,导致小鼠出现强迫性进食行为,即明知存在风险,仍要选择获取食物。为理解高脂食物引发强迫性进食的机制及探索预防由高脂饮食引起的肥胖提供了科学依据。

结果
首先,为研究高脂饮食(high-fat diet, HFD)小鼠的强迫进食行为,研究者训练小鼠按压杠杆以获取蔗糖奖励,随后,引入恐惧条件反射,即在按压获取蔗糖奖励的同时,会有50%的概率出现灯光线索(conditioned stimulus, CS)耦联的足底电击刺激(图1a)。结果显示,在蔗糖奖赏和电击恐惧刺激同时存在的情况下,正常喂养小鼠按压杠杆的次数相较于仅存在蔗糖奖赏时显著降低,而高脂饮食小鼠按压次数则基本保持不变(图1b-e)。提示了HFD可诱发小鼠产生强迫进食行为。
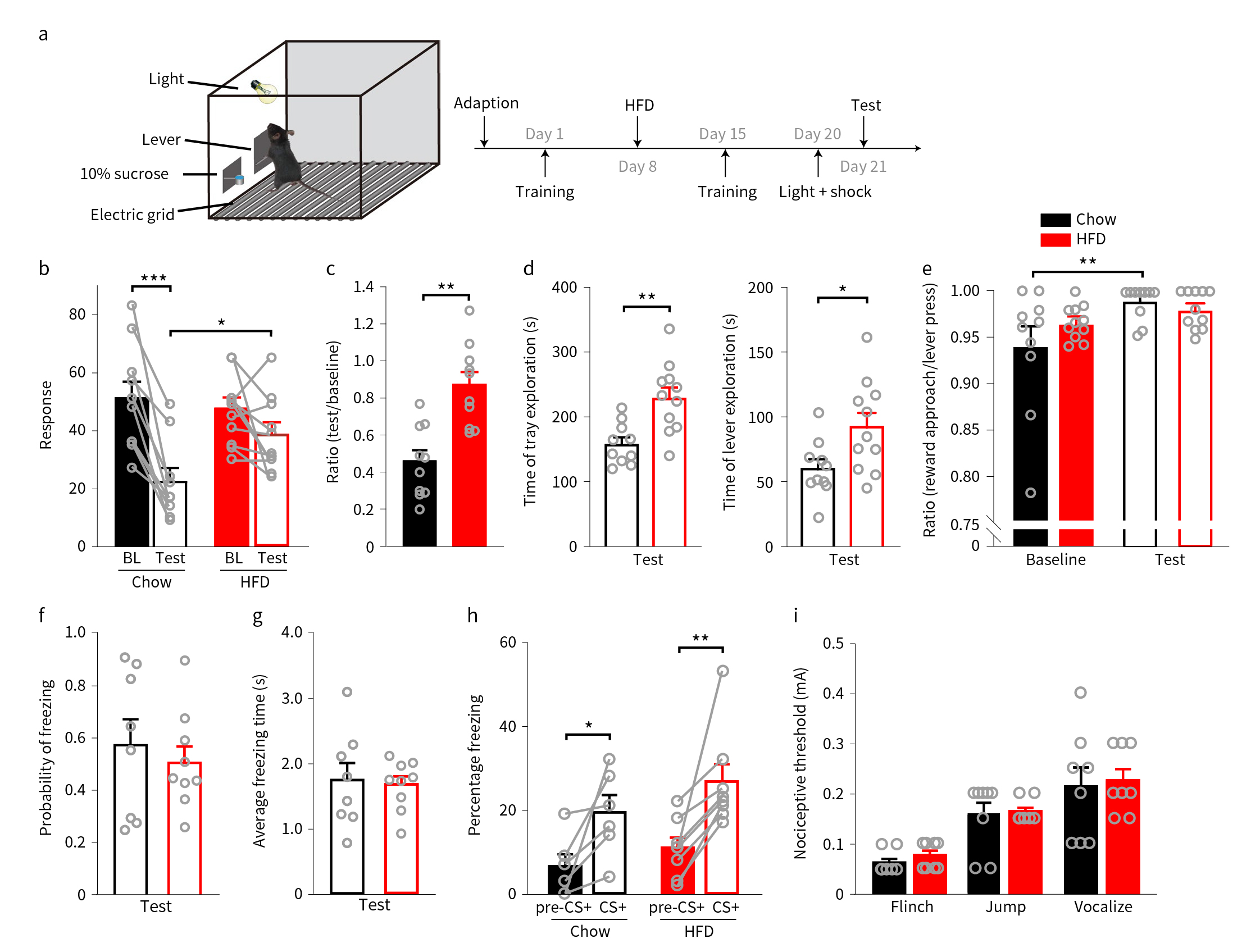
图1 HFD可诱发小鼠产生强迫进食行为
接下来,研究者探讨了高脂饮食诱发小鼠产生强迫进食行为的神经机制,借助c-fos染色发现HFD小鼠丘脑室旁核前侧(anterior paraventricular thalamus, aPVT)在强迫摄取蔗糖过程中CaMKIIα神经元异常激活(图2a-d)。随后,借助在体光纤记录发现,只有当HFD小鼠在强迫进食(按压杠杆获取蔗糖奖励的同时,也伴随着灯光线索耦联的足底电击刺激)过程中,aPVT CaMKIIα神经元活动明显增加(图2e-h)。
进一步,研究者在正常饮食小鼠aPVT注射AAV-CaMKIIα-ChR2-mCherry病毒,并埋入光纤,发现光遗传学激活aPVT CaMKIIα神经元,可增加正常饮食小鼠在足底电击时的按压杠杆次数;同时研究者借助化学遗传学技术发现,当CNO抑制aPVT CaMKIIα神经元时,可减少HFD小鼠按压杠杆次数(图2i-n)。这些结果提示了小鼠大脑aPVT区兴奋性神经元的活动参与小鼠强迫性进食行为,激活aPVT CaMKIIα神经元可促进小鼠的强迫性摄取糖水行为;抑制aPVT CaMKIIα神经元则减弱小鼠该行为。高脂饮食通过诱导aPVT区兴奋性神经元的活动增强从而引起强迫性进食。
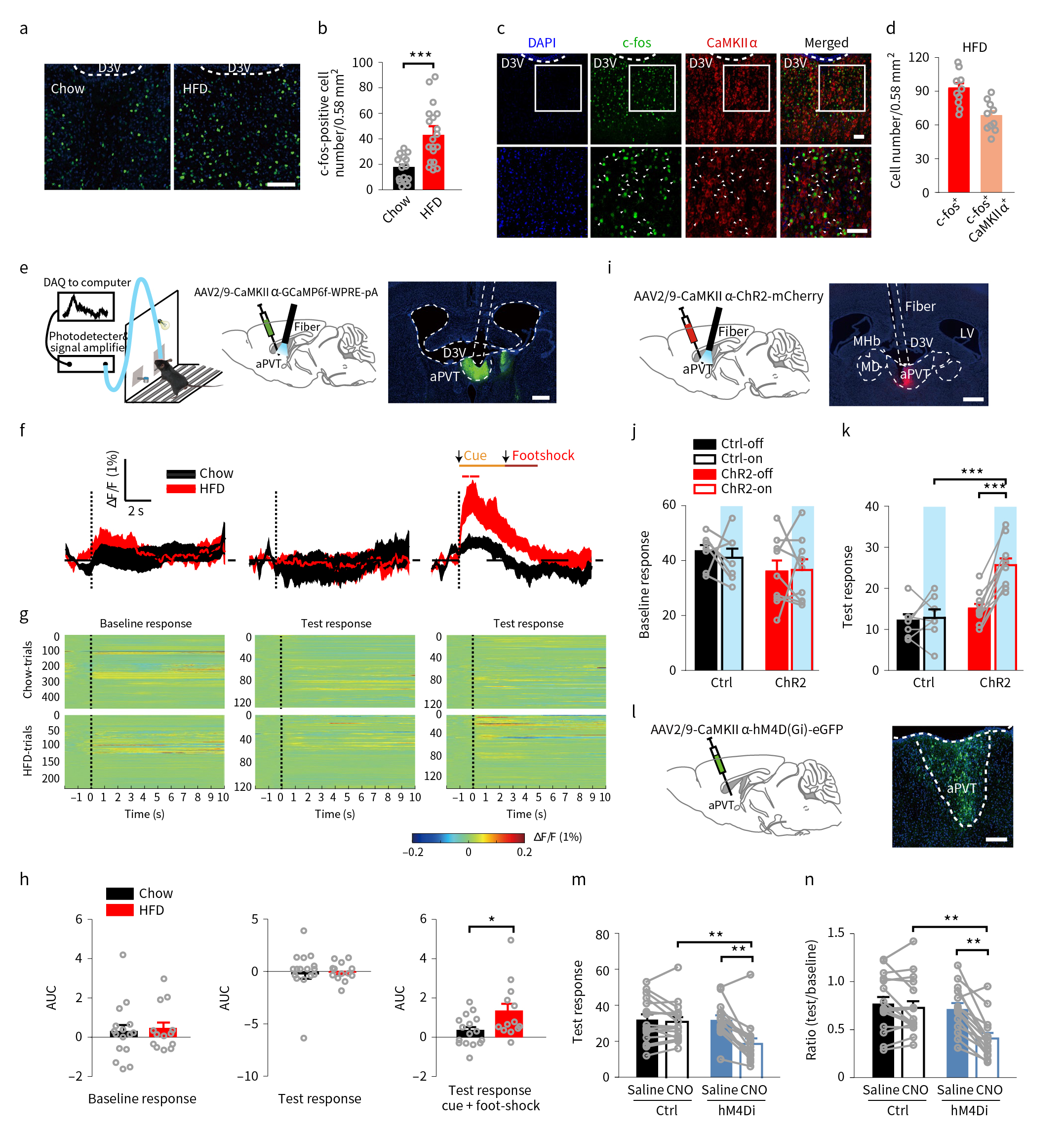
图2 aPVT兴奋性神经元的异常活跃促进小鼠强迫性进食行为
最后,作者研究了HFD诱导aPVT中兴奋性神经元活动水平升高的机制。研究者发现高脂饮食可导致aPVT区小胶质细胞数量显著增多(图3a,b)。通过给予HFD小鼠喂食含有PLX3397(集落刺激因子1受体(CSF1R)抑制剂)的食物发现,HFD小鼠aPVT神经元活动减弱,并缓解强迫性进食行为;此外,研究者将抗CSF-1抗体注射至小鼠aPVT区以特异性减少HFD小鼠aPVT小胶质细胞增生,同样发现HFD小鼠强迫性摄取糖水行为受到抑制(图3c-i)。提示了高脂饮食通过诱导aPVT小胶质细胞激活引发aPVT兴奋性神经元活动水平提升,进而导致小鼠产生强迫性进食行为。

图3 HFD诱导aPVT小胶质细胞激活促进小鼠强迫性进食行为
结论
浙江大学医学院博士生程晶晶、马晓林和博士后李春禄为论文共同第一作者,周煜东教授和沈逸副教授为共同通讯作者。课题受到科技部国家重点研发计划“发育编程及其代谢调节”重点专项和国家自然科学基金的资助。

扫一扫,反馈当前页面
和元生物