
重磅回顾!2015年“魔剪”CRISPR技术重大突破 TOP30

CRISPR作为基因编辑领域的明星技术俨然已经成了众多突破研究的“得力助手”。从技术改良、疾病治疗到作物改良,越来越多的科学研究离不开这项才进入科研领域短短几年的技术。张锋、胚胎编辑、George Church等热词让CRISPR在2015年“屡次刷屏”。
笔者从去年开始关注CRISPR技术,可以明显感觉到今年CRISPR技术相关的论文层出不穷。今年,Science、Cell、Nature三大期刊分别在不同的阶段多次推出CRISPR论文合集或讨论文章。一转眼,2015年已接近尾声;本文探索君带大家一起回顾今年CRISPR技术取得的最新突破进展。
1. PNAS:CRISPR协助细胞对抗HIV(12月14日)
宿主细胞在面对病毒感染的时候,会表达一系列对抗病毒的蛋白,这些蛋白被称为宿主限制因子。哺乳动物细胞编码的限制因子,可以限制HIV-1和其他病毒的复制。不过,被病毒感染的细胞往往不表达这样的限制因子。人们普遍认为,诱导宿主限制因子的表达是抑制病毒复制的一个潜在途径。
杜克大学的Bryan R. Culle领导研究团队在CRISPR/Cas9的基础上构建了转录激活子,成功让人类细胞表达了自己缺乏的限制因子(A3G和A3B)。这项研究发表在12月14日的美国国家科学院院刊PNAS杂志上。
2. Science:张锋再发重大突破,新成果“剑指”CRISPR脱靶效应(11月30日)
11月30日,发表在《科学》杂志上的一项研究中,麻省理工学院-哈佛医学院Broad研究所CRISPR大神张锋的研究小组又取得了一项突破性的成果。研究人员通过创建了3个新版本的Cas9酶大大降低了CRISPR/Cas9系统的脱靶效应;有效改善了这一技术的最大局限性之一。
张锋的团队通过改变构成化脓性链球菌Cas9酶的约1,400个氨基酸中的3个氨基酸将“脱靶编辑”显著减少至无法检测到的水平。他说,不同于其他降低CRISPR/Cas9系统错误率的方式,这些新酶的使用不需要改变许多研究人员现在参照的CRISPR/Cas9系统的protocol。
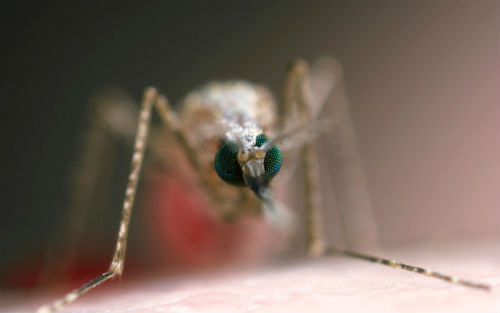
3. PNAS:CRISPR与基因驱动完美结合,改造蚊子有望终结疟疾传播(11月23日)
11月23日 ,美国科学院院报(《PNAS》)期刊发表了一篇利用基于CRISPR/Cas9基础的基因驱动技术实现抗虫基因在蚊子群体的繁衍,从根源上有效阻止疟疾的传播。相比于过去的研究,基因驱动的优势在于,改造过的突变蚊子繁衍的后代都会携带有抗虫基因。
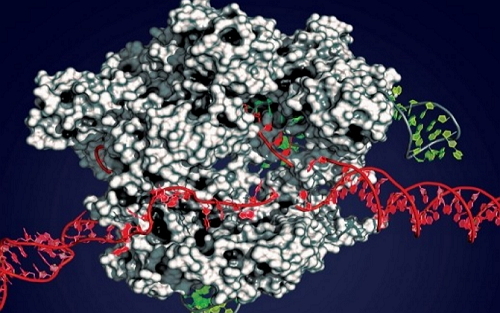
4. Science:破解关键酶Cas9识别全基因组中靶标的重要机制(11月13日)
11月13日,发布在《科学》杂志上的一项研究中,科学家们破解了关键酶Cas9识别全基因组中靶标的重要机制,这将有助于更有效的完善CRISPR基因编辑技术。领导这一研究的是加州大学伯克利分校Jennifer Doudna教授。这些发现揭示了Cas9蛋白在基因组中进行搜寻的机制,表明Cas9的快速“跳过”机制是确保CRISPR作用的前提,这一新见解将有助于完善CRISPR基因编辑技术。
5. Stem Cell Reports:CRISPR与细胞重编程的完美结合(11月12日)
11月12日,发表在《 Stem Cell Reports》上的一项研究中,Morgridge研究所和Murdoch儿童研究所(MCRI)的研究人员,将重编程与CRISPR基因组编辑结合到一个步骤中,显著缩短了生成基因校正干细胞的时间,是实现个性化细胞疗法的重要一步。
6. Cell:揭秘大肠杆菌CRISPR-Cas系统作用机制(11月5日)
11月5日,发布在《细胞》杂志上的一项研究中,科学家们揭示出了大肠杆菌CRISPR-Cas系统监视及加工外源DNA的机制。哥伦比亚大学的Eric C. Greene博士及加州大学伯克利分校的Jennifer Doudna博士是这篇论文的共同通讯作者。
研究结果确立了Cas1-Cas2是在逃避靶标处招募及调控Cas3的一个反式作用因子。基于研究结果,作者们提出了一种Cascade、Cas1、Cas2和Cas3协同作用加工且使得外源遗传元件丧失功能的机制。

7. Nature:揭示CRISPR/Cas9的DNA靶向切割机制(10月28日)
10月28日,发布在《自然》杂志上的一项研究中, 科学家揭示出,Cas9 的HNH核酸酶结构域构象状态直接控制了DNA切割活性。领导这一研究的是加州大学伯克利分校的Jennifer Doudna博士。这些研究结果不仅提供了有关Cas9审查DNA机制的基本认识,对于Cas9作为一种基因工程技术的应用也具有重要的影响。
8. Nature:女神解秘CRISPR/Cas作用机制(10月21日)
10月21日,发布在Nature杂志上的论文中,Jennifer Doudna研究小组揭示出了在CRISPR–Cas适应性免疫中获取外源DNA的机制。研究人员报告称获得了大肠杆菌Cas1–Cas2复合物结合同源33个核苷酸的前间隔序列(protospacer) DNA底物的X-射线晶体结构。这一蛋白质复合物构建出了一个跨越DNA长度的弯曲结合平面,展开前间隔序列的末端使得每个末端亲核3′-OH能够进入到一个通往Cas1活性位点的通道中。磷酸二酯骨架与前间隔序列和蛋白质互作,可以解释在体内观察到的序列非特异性底物选择。这些结果揭示了获取外源DNA的结构基础,及Cas1–Cas2作为分子尺指定CRISPR位点序列结构的机制。
9. Molecular Cell:第二类CRISPR-Cas基因组编辑系统(10月 22日)
一个国际CRISPR-Cas研究人员小组发现了自然存在的、具有基因组编辑潜力的三个新系统。发现以及确定 这些系统的特征有望进一步扩大基因组编辑工具箱,为生物医学研究开辟新的途径。这项研究发表在10月 22日的《分子细胞》(Molecular Cell)杂志上。
10. Cell:揭秘CRISPR“中心法则”,一图了解CRISPR系统作用全步骤(9月24日)
9月24日,来自蒙大拿州立大学的两位学者在《细胞》杂志上以“CRISPR-RNA-Guided Adaptive Immune Systems”为题,介绍了CRISPR-Cas免疫应答系统。其中Blake Wiedenheft就是当年加州大学伯克利分校Jennifer Doudna研究组成员,他们曾于2010年破解了Csy4核糖核酸内切酶原子水平的晶体结构模型。

11. Cell:基因编辑家族“新神器”诞生,CRISPR/Cpf1让一切皆有可能(9月25日)
9月25日,发表在《细胞》杂志上的一项研究中,CRISPR技术先驱、Broad研究所合成生物学家张锋领导的研究小组找到一种让该技术更简单、更精准的方法。伦敦帝国学院的表观遗传学家Luca Magnani说:“这个新发现让很多我们之前不能实现的事情变成了可能。”
12. Nature:张锋发布CRISPR新成果,开辟镰状细胞病治疗新途径(9月16日)
9月16日,来自Dana-Farber/波士顿儿童医院癌症及血液疾病中心的研究人员发现,改变一小段DNA可以避开镰状细胞病(SCD)背后的遗传缺陷。这一发布在《自然》(Nature)杂志上的新发现,为开发出一些基因编辑方法来治疗SCD和诸如地中海贫血等其他的血红蛋白疾病开辟了一条途径。
13. Nature Methods:双功能CRISPR-Cas9,可同步实现基因编辑和调控(9月7日)
9月7日,发表在《Nature Methods》杂志上的一项研究中,哈佛大学和麻省理工的研究团队开发了双重功能的CRISPR-Cas9系统,能够同时实现基因组编辑和基因调控。
14. NEJM新突破:基因编辑神器CRISPR或可逆转肥胖(9月3日)
MIT和哈佛医学院的研究团队发现了一个控制人体代谢的重要通路,操纵这一通路可以改变脂肪细胞的功能。9月3日,这项研究发表在顶级医学期刊《新英格兰医学》上,为人们提供了一条预防和治愈肥胖的新途径。
15. Cell Stem cell:李劲松课题组用CRISPR构建多重基因修饰小鼠(7月9日)
7月9日,发表在《Cell Stem cell》杂志上的一项研究中,来自中科院上海生命科学研究院的研究人员报告称,他们找到了一种方法来提高利用小鼠孤雄单倍体胚胎干细胞系(AG-haESCs)生成半克隆小鼠的效率。并证实借助于CRISPR-Cas9技术可构建出多重遗传修饰的半克隆小鼠及实现对其的诱变遗传筛查。
16. Science:CRISPR女神发表新成果(6月26日)
来自加州大学伯克利分校、德国马克斯普朗克生物物理化学研究所的研究人员揭示出了为识别靶DNA,预先组织形成的一种Cas9-导向RNA(gRNA)复合物的构象。这项研究发布在6月26日的《科学》(Science)杂志上。文章的通讯作者是加州大学伯克利分校的Jennifer A. Doudna博士。
17. Nature:进化中的CRISPR技术又有新突破(6月22日)
来自哈佛医学院和麻省总医院的研究者们在6月22日的Nature杂志上发表了他们新改进的CRISPR-Cas9技术,识别序列的范围更大,识别也更为精准。[详情]
18. Cell:CRISPR揭示惊人发现,百种蛋白都听命于谁?(6月18日)
6月18日发表在《细胞》杂志上的一项研究中,来自加州大学圣地亚哥医学院的研究人员获得了一个令人惊讶的研究发现:100多种分泌蛋白的磷酸化作用都受到一个叫做Fam20C的酶的支配。为了深入探讨Fam20C对人类健康和疾病所起的作用,Dixon研究小组利用了一种新的流行基因编辑技术CRISPR/Cas9来删除了实验室培养的肝癌、乳腺癌和骨癌细胞中的Fam20C基因。
19. Nature技术突破:光控CRISPR-Cas9系统(6月15日)
发表在6月15日《自然生物技术》杂志上的一项研究中,来自日本的研究人员报告称他们构建出了更好的CRISPR基因编辑系统:一种光激活的新型Cas9核酸酶使得研究人员能够在空间和时间上更好地控制RNA引导的核酸酶的活性。
20. Nature子刊:CRISPR可销毁“转基因”生物中特定序列(5月19日)
英国《自然•通讯》杂志5月19日在线发表了一篇合成生物学论文,描述了一种基于“基因组编辑”CRISPR技术的的装置,能销毁转基因生物中特定的DNA序列。控制住特定DNA序列销毁的能力,其应用范围将包括防止转基因生物的环境释放、帮助生物技术公司保护知识产权以及避免偷窃等等。

21. Nature:大师级牛人用CRISPR构建癌症类器官(4月29日)
用含有干细胞巢蛋白(WNT、R-spondin、表皮生长因子EGF)的培养基,可以长期培养小鼠和人类的肠道干细胞,生成遗传学和表型稳定的上皮类器官。荷兰艺术与皇家科学院主席、美国国家科学院院士Hans Clevers教授领导研究团队,利用CRISPR/Cas9技术建立了结直肠癌(CRC)类器官。这一研究成果发表在本周的Nature杂志上。
22. Protein & Cell:中国“80后副教授”基因编辑人类胚胎,争议再升温(4月18日)
4月18日,来自中国中山大学生命科学学院的“80后副教授”黄军就在《Protein & Cell》杂志上首次发表了编辑人类胚胎相关的论文。据Nature新闻描述,这属世界首例,也证实了先前关于有人已经在开展人类胚胎基因编辑研究的传闻。
23. Nature技术突破:将CRISPR效率提高19倍(3月23日)
CRISPR/Cas系统可以构建出多个基因精确突变的小鼠,但其效率低下阻碍了生成足够数量的转基因小鼠来建立人类疾病模型。通过添加一种抗癌药物Scr7到遗传编辑的受精卵中,科学家将CRISPR/Cas的效率显著提高了19倍。这一重要的成果发表在3月23日的《自然生物技术》杂志上。
24. Nature Communications:用CRISPR技术根除艾滋病毒(3月10日)
3月10日,发表在《自然通讯》(Nature Communications)杂志上的一项研究中,来自Salk生物研究所的科学家们通过定制许多细菌利用的一种强大的防御系统(CRISPR),并训练这一剪刀样机器来识别HIV病毒,朝着研发出这样的一种药物迈近了一步。
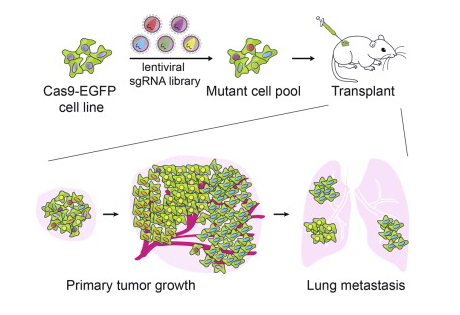
25. 张锋又一篇Cell:让CRISPR在癌症领域大放异彩(3月5日)
一次CRISPR-Cas9基因编辑技术被用于整体生物模型中系统地靶向基因组中的每一个基因。来自Broad研究所和麻省理工学院David H. Koch综合癌症研究所的一个科学家小组,率先利用这一技术在一个癌症动物模型中系统地“敲除”(关闭)了整个基因组的所有基因,揭示出了与肿瘤进化和转移相关的一些基因,这为在其他细胞类型和疾病中从事类似的研究铺平了道路。这项研究工作在线发表在3月5日的《细胞》(Cell)杂志上。
26. Cell:用CRISPR构建衰老研究模型(2月12日)
斯坦福大学的科学家们找利用一种基因组编辑工具箱构建出了可在自然短寿的非洲青鳉鱼中研究衰老的平台。研究人员希望这些鱼将成为了解、预防及治疗老年疾病的一个有价值的新模型。他们将这项研究工作发布在2月12日的《细胞》(Cell)杂志上。
27. Nature Methods: 新方法终结CRISPR-CAS9争论(2月9日)
2月9日,发表在《Nature Methods》上的一项研究中,科学家们成功证实CRISPR-Cas9在人类细胞中有精确的打靶作用,他们开发出一种强大、敏感、无偏见和具有成本效益的方法——Digenome-seq,可在全基因组范围内检测人类细胞中的CRISPR/Cas9脱靶效应。
28. Cell Stem Cell:华人科学家发布新成果,大大提高CRISPR效率(2月5日)
2月5日,发表在《细胞干细胞》杂志上的一项研究中,Gladstone研究所的科学家们发现了一种有效提高CRISPR技术效率的方法。通过与斯坦福大学的同事进行合作,研究人员鉴定出两种小分子化合物能够显著提高插入细胞DNA中的新遗传信息。
29. Nature Biotechnology:精确检测CRISPR脱靶效应的新方法(1月19日)
CRISPR和TALENs作为新兴的基因组编辑技术,虽然优势多多,但是仍然被脱靶效应所困扰。美国希望之城贝克曼研究所和浙江大学第一附属医院的研究人员开发出一种新策略,有望帮助人们检测这种意想不到的结果。这项成果于1月19日在线发表于《Nature Biotechnology》杂志上。
30. Cell:华人学者发布CRISPR重要成果——scRNA(1月15日)
日前,加州大学的科学家们开发了一种CRISPR支架RNA(scRNA)。scRNA编码了靶位点和调控功能,能同时实现对不同基因的激活和抑制。这项研究发表在1月15日的Cell杂志上。
本文转载自生物探索
