胰岛素抵抗是导致2型糖尿病的一个重要原因。证据显示,肥胖是导致胰岛素抵抗的最常见的因素之一[1]。促炎巨噬细胞(M1)分泌的细胞因子TNF-α被认为是肥胖引起的组织炎症的一个原因[2]。利用TNF-α抗体使其与TNF-α结合,发现对胰岛素抵抗和糖代谢的症状改善有限。因此,科学家相信一定存在其他的巨噬细胞和免疫细胞因子对胰岛素敏感起重要作用。美国科学家Jerrold M. Olefsky团队发表在《Cell》杂志上的文章“Adipose Tissue Macrophage-Derived Exosomal miRNAs Can Modulate In Vivo and In Vitro Insulin Sensitivity”,为我们进一步揭示了肥胖导致2型糖尿病的机制。作者研究了脂肪组织巨噬细胞(ATM)分泌的外泌体携带的miRNAs调节细胞胰岛素功能、系统性胰岛素敏感的作用。
要点
1、脂肪组织巨噬细胞(ATM)分泌的外泌体(Exos)将miRNA转移至胰岛素靶细胞
2、肥胖小鼠ATM的Exos可以引发正常小鼠的胰岛素抵抗症状
3、正常小鼠ATM的Exos可以改善肥胖小鼠的胰岛素抵抗症状
4、肥胖小鼠ATM的Exos含有的miR-155可以导致胰岛素抵抗
结论
01 ATMs分泌外泌体并携带miRNAs
首先,研究者对ATM分泌的外泌体进行了分离鉴定,并发现巨噬细胞分泌的miRNA可以转移到目的细胞(Fig.1)。
图 1. 巨噬细胞分泌外泌体miRNA
02 肥胖ATM-Exos促进胰岛素抵抗
其次,研究人员对ATM分泌的外泌体对胰岛素调节的影响进行了研究。通过对正常小鼠分别注射PKH26标记的肥胖或正常小鼠ATM来源的外泌体,研究发现小鼠的肝脏、脂肪和肌肉组织中都检测到PKH26红色荧光信号,与注射正常ATM-Exos相比,注射肥胖ATM-Exos的小鼠,葡萄糖耐受和胰岛素敏感都有不同程度的损伤(Fig.2a-b)。肥胖ATM-Exos处理小鼠,葡萄糖输注率较低(GIR),全身性胰岛素敏感显著降低,胰岛素刺激的葡萄糖输注率(IS-GDR)降低,胰岛素抑制肝脏葡萄糖分泌(HGP)能力和游离脂肪酸(FFA)循环水平也不同程度下降(Fig.2c-f)。另外,受胰岛素调控的AKT磷酸化水平降低,这些组织的胰岛素信号通路也同样受到抑制(Fig.2g-i)。综上结果表明,肥胖小鼠ATM-Exos的miRNA能够损害机体内胰岛素靶器官的胰岛素敏感。
图 2. 含有Exos的肥胖ATM-miRNA导致胰岛素抵抗
03 肥胖ATM-Exos损害胰岛素敏感
科研人员同时对相关的胰岛素靶细胞:脂肪细胞、肌细胞和肝细胞进行了研究。研究发现,肥胖ATM-Exos处理降低3T3-L1脂肪细胞和L6肌细胞的葡萄糖摄取能力,肥胖ATM-Exos阻断肝细胞胰岛素抑制胰高血糖素刺激的肝葡萄糖产生(Fig.3a-c)。肥胖ATM-Exos处理降低了三种胰岛素靶细胞的胰岛素诱导的AKT磷酸化激活(Fig.3d-f)。分别利用对照巨噬细胞外泌体或Drosha敲低的巨噬细胞外泌体对3T3-L1细胞,发现M1巨噬细胞抑制胰岛素刺激的葡萄糖摄取,miRNA减少的M1巨噬细胞则对胰岛素诱导的葡萄糖摄取没有影响(Fig.3g)。以上结果表明,miRNA是巨噬细胞分离的外泌体影响胰岛素靶细胞胰岛素敏感的关键物质。
图 3. 肥胖ATM-Exos调节靶细胞中的胰岛素作用
04 健康小鼠ATM-Exos改善肥胖诱导的胰岛素抵抗
接下来,研究人员对正常ATM-Exos对肥胖引起的胰岛素抵抗的作用进行了研究。对肥胖小鼠利用正常ATM-Exos进行治疗两周后,肥胖小鼠的胰岛素和糖耐受都趋于正常(Fig.4a-b)。正常ATM-Exo提高GIR、IS-GDR和增加胰岛素抑制HGP能力,从而改善高脂饲喂小鼠的胰岛素敏感程度(Fig.4c-e),FFA没有显著变化(Fig.4f)。另外,体外实验与体内实验结果一致,正常ATM-Exos处理促进了胰岛素刺激的3T3-L1和L6细胞的葡萄糖摄取(Fig.4g-h)。以上实验结果说明,正常ATM-Exos的miRNA对肥胖引发的胰岛素抵抗起改善作用。
图 4. 正常小鼠ATMs-Exos可减轻肥胖引起胰岛素抵抗
05 肥胖诱导ATM-Exo-miRNAs表达变化
为了研究肥胖对ATM-Exos miRNA表达的影响,科研人员对肥胖和正常ATM-Exos的miRNA表达进行差异分析,从中筛选出表达差异最大的20种miRNA(Fig.5a)。有研究报道,在其中鉴定出的miRNA中,miRNA-155通过直接抑制PPARγ影响脂肪细胞分化。研究结果显示,肥胖小鼠ATM中miR-155的是正常小鼠的三倍(Fig.5b),从而肥胖小鼠外泌体中MiR-155表达高于正常小鼠(Fig.5c)。肥胖ATM-Exos培养3T3-L1、L6和肝原代细胞均可以增加其MiR-155的表达(Fig.5d-f)。
图 5. 肥胖导致ATM-Exo miRNA谱的变化
06 MiR-155损害细胞胰岛素信号
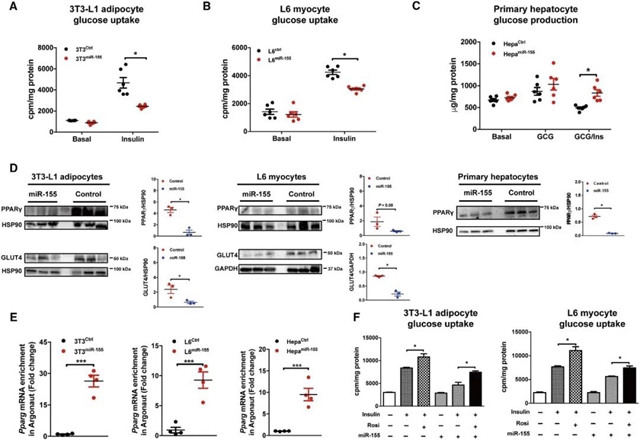
为了进一步研究肥胖ATM-Exos诱导胰岛素抵抗的机制,研究人员对MiR-155胰岛素信号通路的影响进行了研究。miR-155过表达通过降低靶基因PPARγ的表达和GLUT4表达,显著降低了3T3-L1、L6细胞胰岛素诱导的葡萄糖摄取水平;miR-155 mimic转染原代肝细胞,通过减少PPARγ的表达,破坏了胰岛素对HGP的抑制作用(Fig.6a-d)。miR-155过表达后受体细胞中PPARγ mRNA Ago蛋白增加,进一步证明了PPARγ是miR-155的直接靶点(Fig.6e)。研究人员进一步验证了PPARγ激活是否可以恢复miR-155诱导的细胞胰岛素抵抗。结果显示,罗格列酮(PPARγ激动剂)改善了miR-155对3T3-L1、L6细胞胰岛素刺激的葡萄糖摄取的抑制作用(Fig.6f)。
图 6. MiR-155破坏细胞胰岛素作用
07 ATM-Exo-miR-155加重肥胖诱导的胰岛素抵抗
最后,研究人员对miR-155对肥胖引起的胰岛素抵抗影响进行了研究。实验结果显示,miR-155敲除高脂饲喂小鼠相较于单纯高脂饲喂小鼠,肥胖引起的葡萄糖耐受不良和全身性胰岛素抵抗减弱(Fig.7a-b)。
化疗的miR-155KO小鼠分别接受GFP-WT骨髓细胞移植(BMT-WT)和miR-155KO骨髓细胞移植(BMT-miR-155KO)。20周高脂饲喂后,移植鼠体重和GSIS没有明显差异,BMT-WT葡萄糖耐受和胰岛素敏感受损严重(Fig.7c-d)。为进一步确定BMT-WT和BMT-miR-155KO 鼠的胰岛素应答的差异,脂肪细胞和原代肝脏细胞中的miR-155表达减弱,并且其靶基因PPARγ在均减弱(Fig.7e-f)。MiR-155蓄积导致细胞内胰岛素信号受损,通过原代脂肪细胞胰岛素刺激的葡萄糖摄取降低和原代肝细胞胰岛素介导的肝葡萄糖释放抑制增加(Fig.7g-h)。
图 7. miR-155KO小鼠WT骨髓移植促进肥胖诱导的胰岛素抵抗
小结
综上所述,ATM分泌含有miRNA的Exos的影响代谢。肥胖ATM-Exos导致体内和体外胰岛素抵抗,然而,正常ATM-Exos在肥胖小鼠体内产生胰岛素敏感性状态,并在体外增强胰岛素信号转导。研究认为ATM-Exo miRNAs是一种旁分泌和内分泌信号系统,促炎和抗炎ATMs可以影响远端组织的代谢活动。确定其他组织如β细胞、肝细胞或肌细胞产生的外显子是否具有代谢作用产生意义。
参考文献:
[1] Johnson, A.M., and Olefsky, J.M. (2013). The origins and drivers of insulin resistance. Cell 152, 673–684.
[2] De Taeye, B.M., Novitskaya, T., McGuinness, O.P., Gleaves, L., Medda, M., Covington, J.W., and Vaughan, D.E. (2007). Macrophage TNF-alpha contributes to insulin resistance and hepatic steatosis in diet-induced obesity. Am. J. Physiol. Endocrinol. Metab. 293, E713–E725.
和元生物为代谢相关研究提供整体研究方案,从动物造模、基因筛选、基因操作、病毒包装、生理病理检测、机制探究、到观察验证等一站式服务。用专业、认真、严谨的科学态度为代谢研究助力。