
STTT(IF 52.7)|中国医学科学院肿瘤医院冉宇靓团队揭示胃癌干性“黑手”:ENO1如何让ATP与乳酸联手“喂养”肿瘤?
糖酵解对于维持癌症干性至关重要。活跃的糖酵解通常代表肿瘤的恶性表型,并通常伴随糖酵解酶和代谢底物水平升高;然而,糖酵解影响肿瘤的机制尚不清楚。
·研究背景·
胃癌(GC)是全球癌症相关死亡的第四大原因,在东亚地区发病率较高。尽管治疗有所进步,但由于耐药性强,患者预后仍较差,亟需新型治疗靶点和策略。近年来研究表明,肿瘤代谢重编程尤其是糖酵解与肿瘤干性密切相关,糖酵解异常活跃及其产物(如中间体)增加被视为增强干性和化疗耐药的标志。因此,靶向糖酵解酶(如限速酶HK2、PKM2、LDHA)具有潜在临床价值。
α-烯醇化酶(ENO1)作为糖酵解非限速酶,可加速癌细胞糖酵解,但其在促进糖酵解及驱动肿瘤进展中的具体作用研究较少。ENO1同时具有多功能“月光”特性(如扰乱脂质代谢、影响信号通路),作者前期工作已初步证实ENO1通过提升糖酵解增强GC干性。然而,糖酵解在正常细胞中普遍存在,完全抑制风险高,且糖酵解影响肿瘤的具体机制不清。
PI3K/AKT信号通路作为调控细胞代谢和生长的核心通路,在肿瘤中频繁过度激活,其抑制剂虽有初步疗效,但易产生代谢适应性耐药,亟需联合靶向代谢的策略。本研究基于此,进一步探讨ENO1通过糖酵解调控ATP水平和乳酸稳态,影响PI3K/AKT及AMPK/mTOR通路,从而驱动GC干性的详细机制,为多节点联合治疗提供新方向。
·研究结果·
1.ENO1在胃癌中上调表达与患者不良预后及干细胞样特性相关
探讨ENO1在胃癌(GC)中的表达情况,作者使用人胃癌组织芯片进行免疫组织化学(IHC)分析。与癌旁正常组织相比,胃癌组织中ENO1的核质表达均显著升高(图1a)。此外,对特征均衡的胃癌患者进行ENO1表达分层生存分析显示,高ENO1表达患者的生存率显著低于低表达患者(图1b),且在核ENO1低表达患者中,胞质ENO1表达水平也影响生存。随后作者使用慢病毒构建PAMC82和SNU16细胞系的ENO1差异表达细胞模型,发现ENO1上调对细胞增殖无显著影响,但促进球形成(图1c)、迁移(图1d)、侵袭能力以及干性因子表达(图1e),而ENO1敲低(shENO1)胃癌细胞则呈现相反趋势。此外作者建立了小鼠模型,发现高ENO1表达显著增加肺转移并导致肺重量增加。由于转移结节过多,可能导致肺功能受损、系统性缺氧,进一步影响整体代谢和生理功能,最终导致裸鼠体重略微下降(图1f)。综上,这些结果表明高ENO1表达可能与胃癌患者不良预后及胃癌细胞干细胞样特性相关。
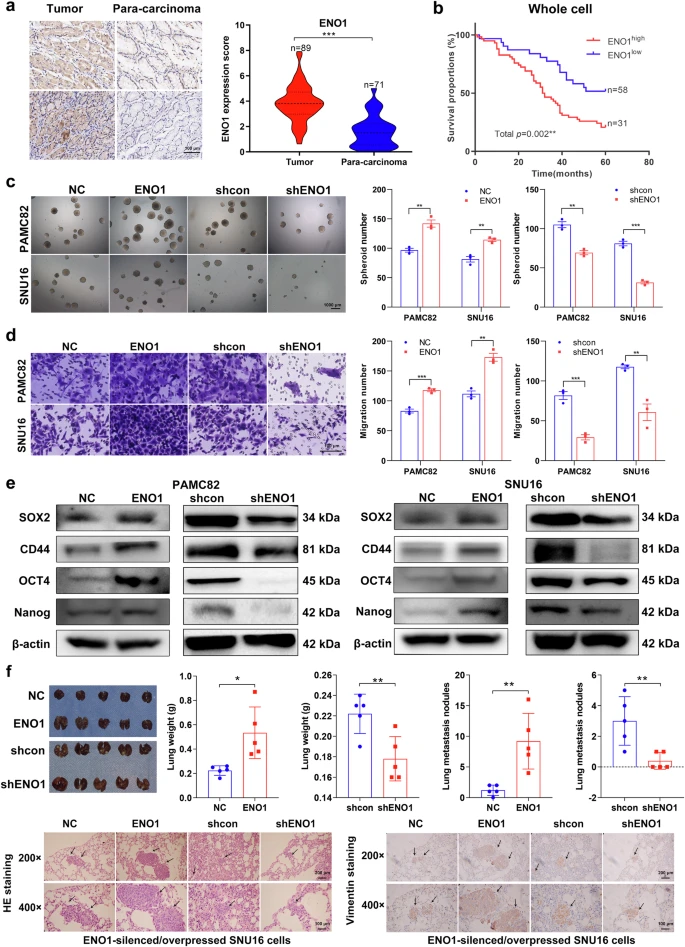
图1 ENO1高表达与患者不良预后及GC干性特征相关
2.高ENO1通过介导PI3K/AKT激活和AMPK/mTOR失活增强胃癌干性
作者对对照组和ENO1敲低组进行了RNA-Seq分析,结果显示:敲低组细胞中共有2116个基因上调、1845个基因下调(图2a);KEGG 和GO分析显示:差异表达基因(DEGs)主要富集于代谢通路,如糖酵解过程的正调控和AMPK/mTOR信号(图2b、c);GSEA分析进一步显示ENO1可能介导AMPK/mTOR通路(图2d)。
为进一步探究ENO1是否在PI3K/AKT通路(糖酵解的经典调控通路)中发挥功能作用,作者进行了WB 验证后发现ENO1差异表达显著改变AKT/mTOR通路和AMPK的磷酸化状态(图2e)。接着作者使用PI3K抑制剂LY294002和激活剂740Y-P验证ENO1是否通过PI3K/AKT通路影响干性。正如预期那样,LY294002逆转了ENO1过表达诱导的PI3K/AKT通路激活(图2f),表现为AKT和mTOR磷酸化减少;相应地,ENO1过表达组在LY294002处理后球形成、迁移和侵袭能力被显著抑制(图2g;补充图2c)。同样,在shENO1胃癌细胞中加入740Y-P后观察到p-AKT和p-mTOR表达增加,提示740Y-P处理可挽救ENO1缺失引起的PI3K/AKT信号抑制;此外,740Y-P逆转了shENO1细胞中自我更新、迁移和侵袭的抑制效应。作者进一步还使用了AMPK激活剂AICAR和mTOR抑制剂雷帕霉素/激活剂MHY1485鉴定ENO1是否可失活AMPK/mTOR通路并影响干细胞样特性。结果显示:AICAR在ENO1过表达细胞中可增加磷酸化AMPK水平,表明ENO1诱导的AMPK/mTOR通路失活被逆转(图2h);并且AICAR还削弱了ENO1过表达胃癌细胞的球体形成、迁移和侵袭能力(图2i)。此外雷帕霉素的效果与AICAR相似,能激活AMPK/mTOR通路并抑制干细胞样特性,而MHY1485则呈现相反趋势。综上,这些结果表明ENO1通过激活PI3K/AKT信号并失活AMPK/mTOR通路来增强干性。
基于上述发现,作者探讨ENO1是否通过协同介导AMPK/mTOR和PI3K/AKT通路调控干性特性,发现AICAR联合LY294002强烈抑制ENO1过表达胃癌细胞的自我更新、迁移和侵袭能力。作者进一步探究了联合信号通路抑制的潜在临床意义,结果显示使用二甲双胍(AMPK激活剂;MET)和copanlisib(PI3K抑制剂;COPAN)联合治疗结果优于单药治疗,即联合治疗显著抑制细胞活力、克隆形成、球体形成、迁移和侵袭。最后作者构建了GC小鼠异种移植模型,结果显示联合组肿瘤体积和重量低于单药组,但差异不显著。因此,旨在寻找更有效的联合治疗策略。综上,这些结果表明高ENO1水平通过协同介导PI3K/AKT激活和AMPK/mTOR失活增强干性,促进胃癌生长。
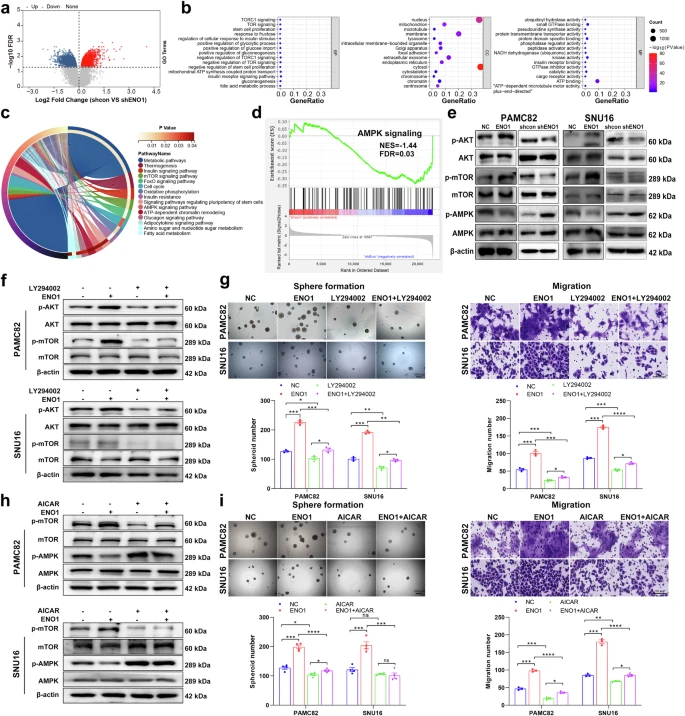
图2 ENO1通过调节PI3K/AKT和AMPK/mTOR通路促进干细胞样特性
3.ENO1通过激活糖酵解增加乳酸和细胞质ATP产生,随后调控PI3K/AKT和AMPK/mTOR通路,最终促进肿瘤转移和干性
由于PI3K/AKT和AMPK/mTOR信号通路是经典的能量代谢相关通路,接下来作者分析了TCGA数据库中的肿瘤样本,发现高表达ENO1的患者呈现更高的糖酵解相关评分(补充图6a)。结合补充图6b的数据,作者对临床胃癌样本的TCGA和RNA-Seq结果分析一致显示ENO1影响两种关键糖酵解产物——ATP和乳酸的水平。
随后,作者对shcon和shENO1组细胞进行能量代谢谱分析。与shcon组相比,shENO1组有21种代谢物上调、13种代谢物下调(图3a)。KEGG富集分析显示差异代谢物主要富集于糖酵解和糖异生通路,特别是糖酵解的正调控(图3b)。糖酵解关键中间代谢物呈现显著差异,ATP和乳酸产生明显减少(图3c、d)。并且作者验证了ENO1促进乳酸和ATP水平升高(图3e)。DEGs和差异代谢物的整合通路分析显示PI3K/AKT和AMPK信号通路显著富集(图3f)。为了进一步验证ENO1诱导的干细胞样特性是否可被逆转,作者用糖酵解抑制剂2-脱氧-D-葡萄糖(2-DG)处理细胞,并检测了PI3K/AKT和AMPK/mTOR通路的调控。结果显示,2-DG降低了ATP和乳酸水平,这与shENO1组的发现一致。ENOblock和2-DG对PI3K/AKT和AMPK/mTOR通路的影响相似,表明ENO1主要通过糖酵解调控这些通路。此外,2-DG逆转了ENO1诱导的胃癌细胞自我更新、迁移和侵袭能力增加。
4.细胞质ATP池升高浓度依赖性地直接激活PI3K/AKT信号,驱动胃癌进展
基于先前研究,作者推断ENO1可通过激活糖酵解并增加ATP和乳酸水平调控PI3K/AKT和AMPK/mTOR通路,从而影响干性。研究结果显示ATP产生与AMPK/mTOR通路激活呈负相关,这与Cancer Cell先前报道一致。作者随后验证了ATP和乳酸对PI3K/AKT信号通路的影响,由于ATP无法自由跨膜扩散,细胞内ATP浓度显著高于细胞外,作者通过膜通透化实验建立不同细胞内ATP浓度的细胞群,观察ATP对PI3K/AKT通路的瞬时影响(图3g),结果显示,在膜通透性增加下,ATP外流导致的ATP泄漏可通过ATP补充部分恢复,PI3K/AKT信号激活随细胞内ATP浓度变化(图3h)。此外,在膜通透化后ATP添加并恢复12 h后,结果显示肿瘤干性相关标记表达发生变化(E-cadherin下调,N-cadherin、vimentin、snail、SOX2、CD44、OCT4和Nanog上调),表明细胞内高ATP水平可通过激活PI3K/AKT信号通路促进胃癌细胞干性,并且结果还显示与迁移、侵袭和干性相关的恶性表型显著增强。
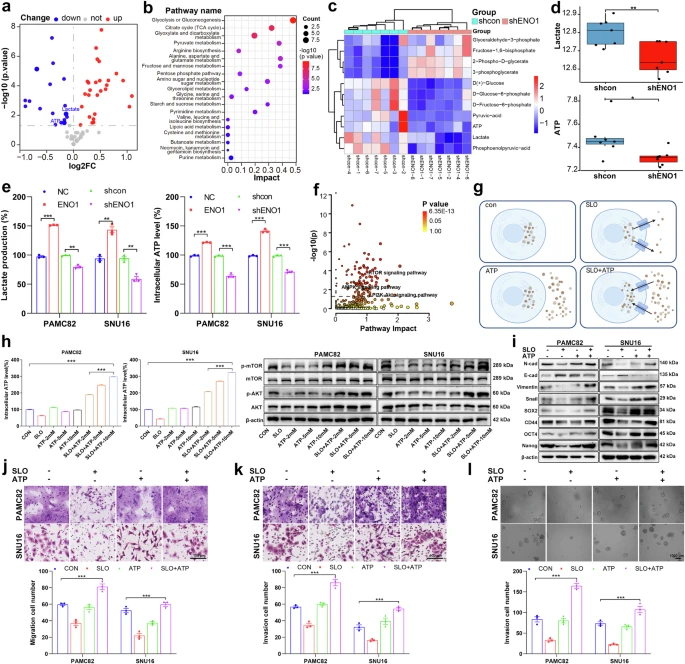
图3 ENO1通过调节乳酸和ATP的产生来激活PI3K/AKT通路,从而促进肿瘤的侵袭和干性
5.细胞内乳酸增加浓度依赖性地促进胃癌侵袭和干性,由糖酵解来源ATP介导的PI3K/AKT通路激活所调控
由于ENO1可调控乳酸产生,为进一步探讨乳酸的功能机制,作者发现外源乳酸补充导致细胞内乳酸水平增加,建立细胞内-外乳酸动态平衡,并促进胃癌细胞迁移、侵袭和自我更新(图4a、b)。Western blot分析提示乳酸增强干性和EMT相关分子表型,从而促进胃癌干性和EMT(图4c)。此外,通过添加不同浓度乳酸钠,胃癌细胞整体乳酰化水平逐步增加(图4e),伴随迁移能力(图4d)、球形成能力(图4d)和干性(图4e)的分子指标逐步增加。这些发现提示乳酸通过调控整体乳酰化水平促进肿瘤细胞干性。
作者进一步探讨了乳酸对PI3K/AKT通路的影响,发现乳酸促进PI3K/AKT通路激活。当乳酸与PI3K抑制剂COPAN共给药时,其相关的迁移和球形成增强(图4f)以及PI3K/AKT通路激活(图4g;补充图9c)显著减弱,表明乳酸的促肿瘤功能依赖PI3K/AKT激活。最后作者分别通过2-DG和oligoA选择性地抑制糖酵解和线粒体ATP的产生,研究结果显示,经过2-DG处理后,外源性乳酸没有增强迁移或球体形成或激活PI3K/AKT通路,而经oligoA处理后出现了相反的结果。这些发现表明乳酸的致瘤作用依赖于糖酵解而不是线粒体来源的ATP。
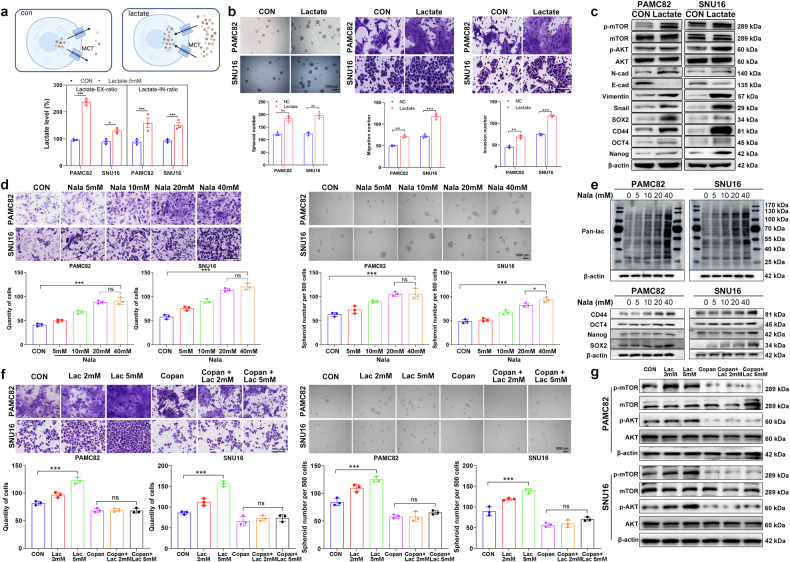
图4 乳酸以剂量依赖的方式促进肿瘤侵袭和干细胞形成,这是通过糖酵解衍生的ATP依赖性PI3K/AKT激活介导的
6.二甲双胍联合昔洛舍平同时靶向ATP池和乳酸稳态协同抑制胃癌细胞干性,从而更有效地抑制肿瘤生长
考虑到细胞质ATP和乳酸的协同作用,作者提出同时靶向两种代谢物的联合治疗。鉴于未来临床应用价值,作者选择两种临床相关药物:二甲双胍(MET)和昔洛舍平(SYRO)。不同浓度MET影响细胞内ATP池,检测到细胞内ATP水平下降但乳酸水平无变化。有趣的是,数据还提出了一种新机制,即MET主要通过糖酵解而不是通过线粒体氧化磷酸化来调节ATP的产生(图5a)。此外,SYRO靶向单羧酸转运体(MCTs)破坏肿瘤乳酸稳态后,细胞外乳酸减少;还观察到ATP不明原因增加,但这种增加并不影响药物对PI3K/AKT通路的抑制作用或AMPK通路的激活。
基于剂量梯度实验的代谢物浓度和对两条通路的影响结果,作者使用MET和SYRO进一步探讨对通路和干性的协同效应。MET和SYRO联合对PI3K/AKT激活和AMPK/mTOR失活的抑制效应较单药更强。体外实验中,联合用药较单药更显著地抑制细胞活力(图5d)、克隆形成(图5e)、球形成(图5f)、迁移(图5g)和侵袭能力。在皮下异种移植瘤模型中,联合组肿瘤体积和重量显著小于单药组,表明联合治疗更有效地抑制肿瘤生长。总的来说,作者得出结论:ENO1通过直接刺激糖酵解产物协同调控PI3K/AKT和AMPK/mTOR通路,并影响ATP池和乳酸稳态,最终促进胃癌的干细胞特性和肿瘤生长(图6)。
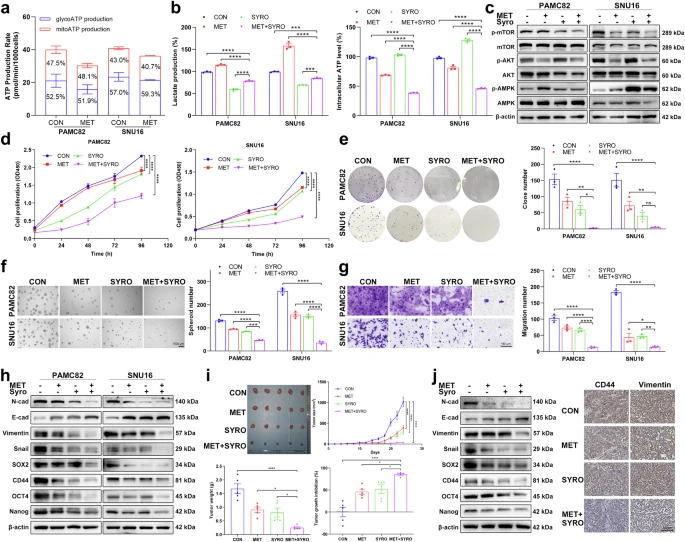
图5 同时靶向ATP和乳酸抑制胃癌细胞的干性和肿瘤生长
·全文总结·
本研究首次系统揭示了糖酵解酶α-烯醇酶(ENO1)通过调控胃癌中糖酵解代谢物的产生和浓度,从而维持肿瘤内恶性信号传导。本文提出了关于癌症代谢综合调控的新见解:ENO1通过增强糖酵解→提升胞内ATP与乳酸水平→ATP直接并协同乳酸激活PI3K/AKT信号、同时抑制AMPK/mTOR信号→最终驱动胃癌干细胞特性与恶性进展。此外,作者通过临床可用药物(MET和SYRO)靶向ENO1-ATP/乳酸-AMPK/PI3K/AKT-mTOR轴上多个节点,为克服传统单一靶点疗法的耐药性问题提供了新的方向,具有明确的临床转化前景。
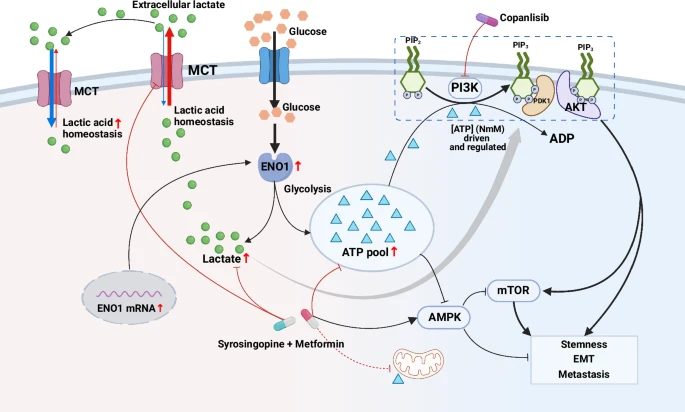
图6 ENO1调控胃癌干性的机制示意图
和元服务
和元一直致力为肿瘤研究提供整体解决方案,从基因筛选、基因功能研究到机制研究,提供质粒构建、病毒包装、基因过表达、基因干扰、基因敲除稳转株构建、细胞功能学实验、双荧光素酶检测服务到动物模型构建一站式技术服务!

更多活动详情可长按或扫描上方二维码,填写表单,我们将尽快安排专人与您联系!
和元生物
上海和元生物技术(集团)股份有限公司(股票代码:688238)作为一家在科创板上市的高新技术企业,自2013年成立以来,始终深耕细胞和基因治疗核心领域,专注于为细胞和基因治疗的基础研究提供基因治疗载体研制、基因功能研究、药物靶点及药效研究等CRO服务,可提供①组学服务:常规转录组、单细胞转录组、基因组、代谢组及蛋白组等。②载体构建和病毒包装:质粒、siRNA、腺相关病毒(AAV)、腺病毒(ADV)、慢病毒(LVV)、逆转录病毒(RV)、单纯疱疹病毒(HSV)等病毒载体生产服务,提供R&D、实验室级别、GMP级别,满足研发、小动物、大动物NHP到临床的不同研究阶段的使用需求。③细胞实验服务:过表达、干扰稳定株构建,单克隆细胞株构建服务及细胞功能学、药效学实验服务。④动物实验及机制研究:神经、代谢、肿瘤动物模型、药效药代、病理切片及蛋白、核酸检测服务。⑤特色项目服务:CRISPR文库筛选服务,外泌体整体研究服务,AAV衣壳筛选服务、听力研究整体项目服务,满足客户定制化或一站式项目服务,助力基础科学研究,促进基础研究到临床转化应用,推动细胞和基因治疗行业发展。

扫一扫,反馈当前页面
和元生物