
【探秘GCT智造】不仅一次性袋子!全流程一次性工艺原核细胞培养工艺解析
文章来自和元生物内容团队,转载请注明出处

揭秘全流程一次性工艺原核细胞培养
随着生物技术进步、全球人口总量持续增长、社会老龄化程度的加剧以及众多未被满足的医疗需求,全球生物医药市场规模稳步发展。但同时,生物制品(尤其如基因细胞治疗产品)由于种类繁多,产品本身高活性、高敏性特质,同时生产工艺路线长、工艺复杂,原辅料种类多等多因素,对产品生产过程无菌风险管控提出了更高的要求。
本月初,国家药监局核查中心发布的《药品共线生产质量风险管理指南》就生物制品针对性地提出了策略指导,肯定了一次性使用技术在避免产品交叉污染中的重要性。

图片来源:
《药品共线生产质量风险管理指南》部分摘取
22年底Reportlinker发布的《全球一次性生物加工市场》报告更准确地指出了,由于不锈钢罐生产工艺在经济上更具规模可行性,目前其在生物药商业化生产中更多地被使用。但同时,在商业化生产前期,基于监管要求、生产灵活性及较小规模的生产需求等多方面的考量,一次性生产工艺系统目前正在主导生物药商业化生产前市场,并逐步扩大在商业化生产中的应用。
为什么提出全流程一次性工艺原核细胞培养(质粒)生产工艺
在一次性生产工艺1.0时代,更多指的仅是一次性上游发酵工艺,也是常被提到的一次性袋子进行大肠杆菌发酵生产质粒。但伴随着上下游供应链的完善,基于QbD理念,全流程一次性工艺原核细胞培养(质粒)生产工艺被提出。
除菌种复苏采用A级保护外,其它工艺步骤如:接种、发酵、菌体收获、裂解、澄清过滤、超滤、层析全过程密闭操作,实现全过程的无菌工艺,完美解决病毒生产用质粒产品、裸质粒产品、菌制剂产品的无菌控制难点。并且由于与产品直接接触的全一次性耗材,不需考虑不同产品间的交叉污染,无需考虑转产过程的残留检测,降低清洁工艺开发难度,避免法规对残留物检测的专属性和灵敏度的挑战,最大限度避免产品间的交叉污染风险。

全流程一次性工艺原核细胞培养(质粒)生产工艺难点在哪里
相较于不锈钢系统的高度自动化,一次性工艺生产由于模块多、组合多,各步骤间通常采用人工手动连接,这对生产稳定性、可控性及合规性带来了不小的挑战。
和元生物基于历史生产经验,针对一次性工艺硬件,设计并独创了相匹配的自动化控制逻辑执行生产过程控制系统,且设备的软件符合CFR Part11法规要求。全过程自动化控制有效保障了生产数据完整性与合规性,同时,减少了人为干扰误差让产品的生产控制具备重复性和稳定性。

和元智造
保质且保量-媲美不锈钢系统的产量
基于和元生物20+批一次性GMP质粒生产经验,从图1可以看到,一次性工艺系统的产量与不锈钢系统基本一致。
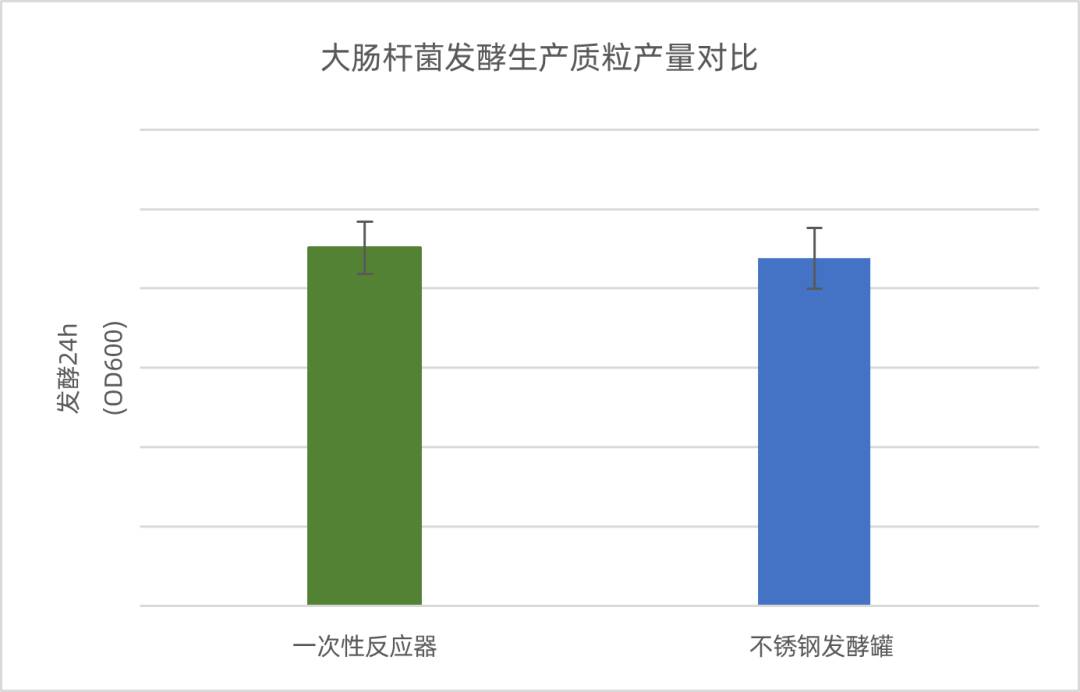
图1 大肠杆菌发酵生产质粒产量对比
但除培养的性能外,在生产中,影响产能的另外一个重要因素是周转率。由于提高周转率,减少清场验证时间,一次性工艺的年生产批次比传统不锈钢发酵罐提高约一倍。
全面、灵活的原核细胞培养(质粒)生产平台
和元生物临港产业基地于上海自由贸易试验区临港新片区建设77,000平方米精准医疗产业基地,基地配备3条可供商业化GMP生产使用原核细胞培养(质粒)生产线,其中包括:一条全流程一次性工艺生产线;一条10L-50L-500L三联罐生产线;一条不锈钢系统生产线。
和元生物CDMO平台基于QbD和BSL-2设计理念,可根据病毒生产用质粒、裸质粒、菌制剂等不同产品生产需求快速提供各种质粒产品、菌制剂产品的解决方案,多种通量的设备,多种模式的灵活设备设施搭配,有效区分活菌区与非活菌区,人流、物流、废物流的独立设计,加快产品转化速度。

COMING SOON
和创新纪元
智愈未来 造就非凡
和元智造精准医疗产业基地开业盛典
2023年4月21日
中国·上海
感谢以下单位支持
香港奥星集团
楚天科技股份有限公司
赛多利斯斯泰帝(上海)贸易有限公司
赛默飞世尔科技(中国)有限公司
上海凯贤流体科技有限公司
上海荟诚信息系统有限公司
上海德卡实验室系统科技有限公司
上海宸芯环保科技有限公司
上海林玮消防工程有限公司
丁之洁团队(现伍德中国生命科学事业部)
Reference:
1.和元生物工艺团队
2.https://mp.weixin.qq.com/s/G87moy6KNxlJsGxuyIXHHQ

扫一扫,反馈当前页面
和元生物